« Deuxième vague » Covid-19 : perspectives 2020–2021

L’utilisation d’Excel appliquée à la version la plus simple du traditionnel modèle SIR de Kermack et McKendrick permet à des non-mathématiciens de modéliser très facilement et de façon fidèle la situation française jusqu’à fin octobre 2020. La correction d’une équation de ce modèle de 1927 améliore la conformité du modèle avec la réalité observée dans cette épidémie, ce qui permet de mieux évaluer les risques d’évolution fin 2020 et début 2021.
Aux lecteurs : prendre connaissance avant de lire cet article de : https://www.lajauneetlarouge.com/covid-19-une-modelisation-simple-utilisant-excel-accessible-aux-non-mathematiciens-et-pleine-denseignements/ (J&R n° 758 d’octobre 2020) en sautant le dernier paragraphe sur l’immunité collective qui est repris de façon plus explicite dans l’annexe 2 du présent article.
Rappel
Dans la version en ligne du n° 758 de La Jaune et la Rouge (octobre 2020) figurent deux articles sur la modélisation mathématique des épidémies.
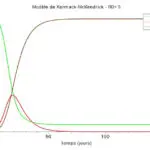
Le deuxième intitulé « Une modélisation simple utilisant Excel … » inclut le diagramme suivant :
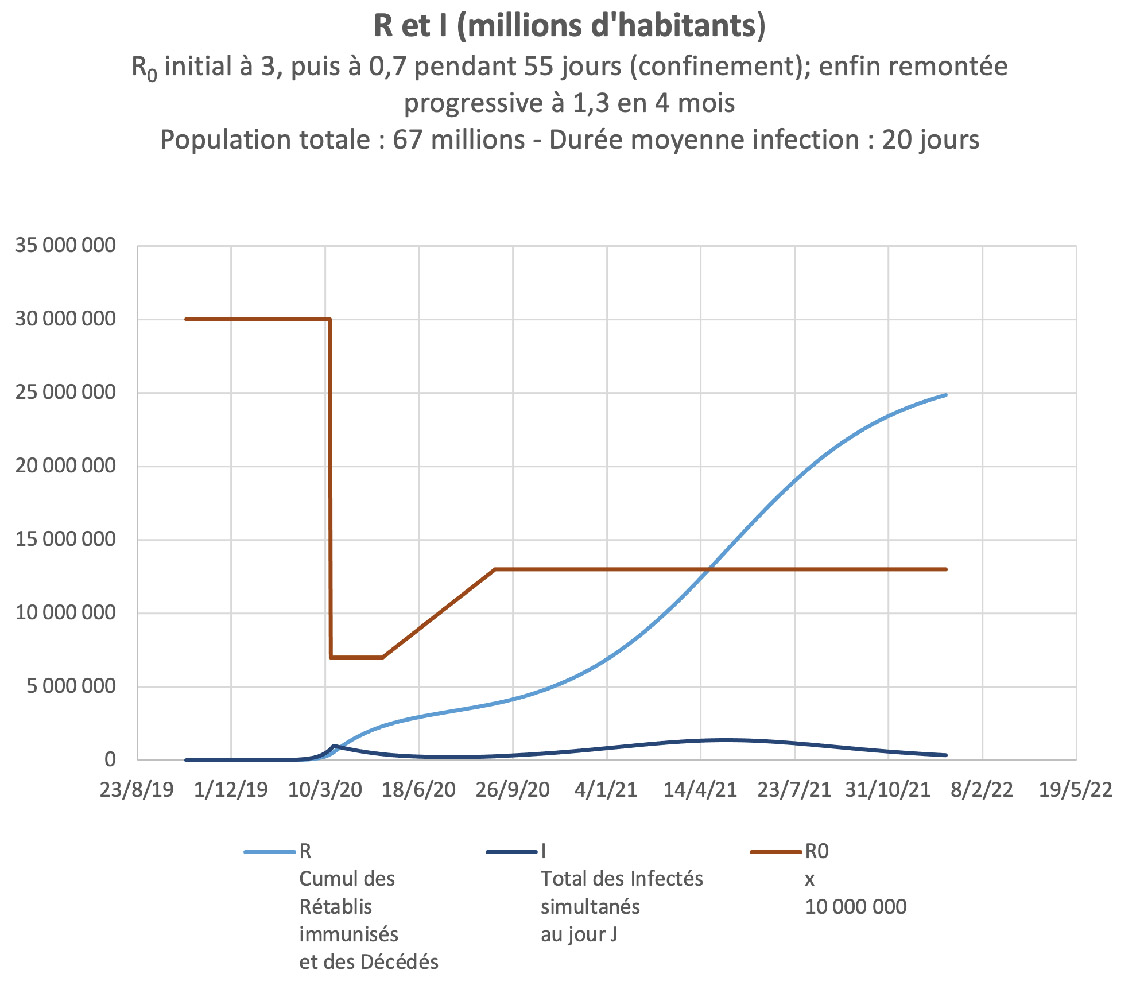
Ce diagramme est basé sur l’utilisation du modèle classique SIR de Kermack et McKendrick et l’hypothèse d’une évolution de R0 passant de 3 avant la pandémie à 0,7 pendant le confinement (17 mars – 11 mai), puis d’une remontée progressive jusqu’à 1,3.
Si R0 se stabilisait ensuite de façon durable à cette valeur de 1,3, on constaterait une remontée de l’épidémie à partir de l’automne 2020 jusqu’au début de l’été 2021, moment où serait atteint le seuil d’immunité collective correspondant à R = 1,3 (voir annexe 2).
« Si R0 se stabilisait de façon durable à cette valeur de 1,3,
on constaterait une remontée de l’épidémie à partir de l’automne 2020
jusqu’au début de l’été 2021. »
Avait été indiqué dans les deux articles de la J&R d’octobre combien l’une des équations de 1927 (utilisée dans tous des cours d’épidémiologie !) paraissait, pour reprendre un qualificatif utilisé dans un autre contexte par le Pr Didier Raoult, « foireuse ». Il s’agit de celle qui rend compte du débit de sortie (par guérison immunisante ou décès) du « compartiment des infectés » qui serait proportionnelle à tout instant au nombre I des infectés divisé par D, durée moyenne de l’infection pendant laquelle les individus sont réputés contagieux.
Si cette approximation est justifiée en régime établi d’arrivée et de sortie d’individus dans I, elle est inexacte en régime dynamique, où elle devrait être remplacée par une équation exprimant que les individus de I qui arrêtent d’être contagieux à l’instant t sont ceux qui ont été infectés à l’instant (t – D), D étant la durée moyenne séparant leur infection de leur guérison ou de leur décès.
Pour prendre en compte cette remarque, il suffit de remplacer dans les équations traditionnelles de 1927 :
dR(t)/dt = γ I (t) (modélisé en utilisant Excel)
par
dR(t)/dt = – dS(t – D)/dt (dont la modélisation via Excel est tout aussi simple)
ce qui, de façon intuitive, correspond beaucoup mieux à la simulation d’un phénomène où tous les individus passent à peu près le même temps dans le « compartiment I ».
Les ordinateurs n’existant pas en 1927, Kermack et McKendrick ont vraisemblablement préféré se raccrocher à la forme classique de la première équation différentielle, ce qui leur a permis, ainsi qu’à leurs successeurs, d’obtenir un certain nombre de conclusions par des méthodes de pur raisonnement mathématique, sans avoir besoin de recourir aux fastidieux calculs manuels itératifs nécessaires à l’époque pour tracer les courbes de S, I et R.
Observations sur le développement de l’épidémie fin octobre 2020
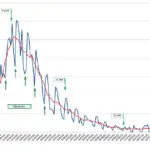
La baisse du nombre de personnes infectées pendant l’été 2020 prévue par le modèle (malheureusement non mesurable, sauf à utiliser des techniques de sondage, ce qui n’a pas été fait pour des raisons inexplicables) a bien été constatée au niveau de ses conséquences sur les hospitalisations et les décès, et a même permis à certains de dire que l’épidémie était en train de s’éteindre d’elle-même. Mais depuis septembre, la situation a beaucoup changé : le nombre de morts Covid dans les hôpitaux, qui est l’information la plus fiable, connaît depuis cette époque une hausse de type exponentiel (voir figure), certes beaucoup plus lente que celle de mars 2020, mais qui néanmoins amène notre pays à déplorer fin octobre plus de 200 décès Covid quotidiens, soit déjà le tiers du pic de la « première vague » survenu une vingtaine de jours après le début du premier confinement.
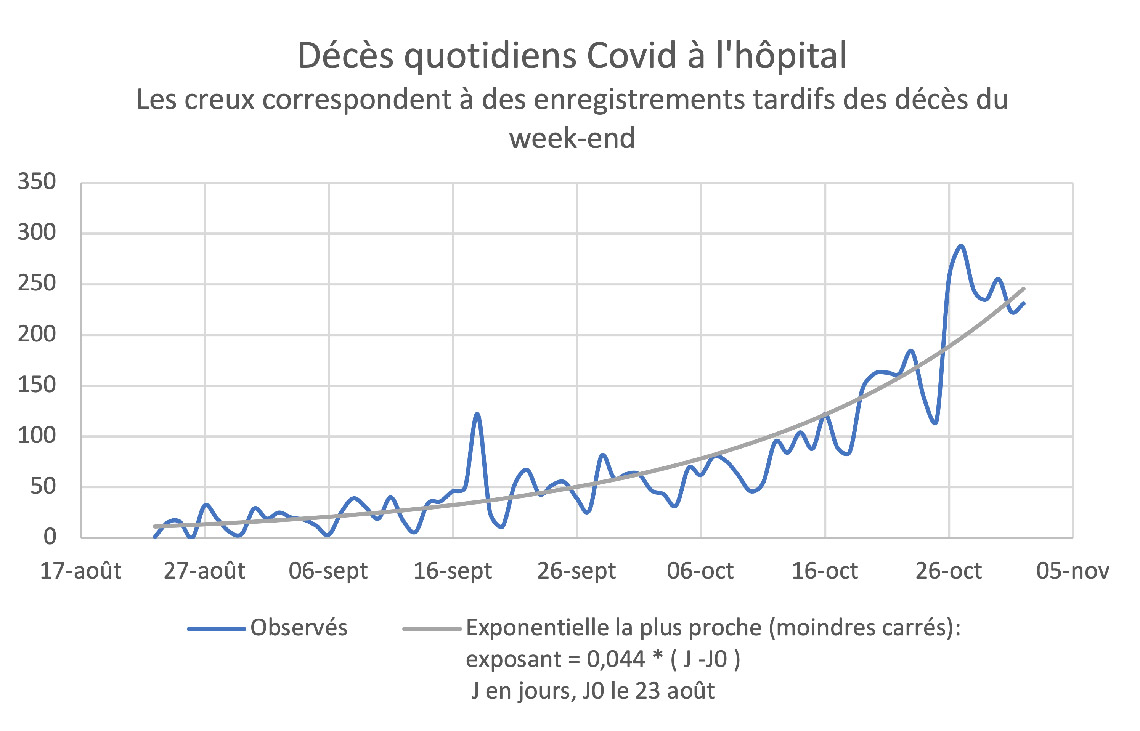
Ceci amène immédiatement deux questions :
- le coefficient R0 serait-il monté au-dessus de 1,3 ?
- que se passe-t-il si on replace l’équation « foireuse » du SIR classique de 1927 par celle suggérée plus haut ?
Montée de R0 au-dessus de 1,3 ?
(une fois de plus, bien noter que la notation traditionnelle R0 n’a rien à voir avec R(0), nombre d’individus dans le compartiment R à l’instant 0).
Rappelons d’abord ce que signifient les différentes versions de R.
R0 est le nombre moyen de cas secondaires produits pendant toute la durée de son infection par un infectieux placé dans une population saine susceptible d’être infectée (donc non vaccinée et ne bénéficiant pas – si ce cas existe – d’une immunité naturelle l’empêchant d’être infectée puis contagieuse).
Rappelons que R0 est égal au nombre quotidien de rencontres potentiellement contaminantes d’un infecté avec n’importe quel autre membre de la population multiplié par la proportion de ces rencontres débouchant sur une infection réelle puis divisé par le nombre moyen de jours entre infection et guérison ou décès.
Reffectif (nombre de reprodution effectif) est égal à R0 à deux conditions :
(voir à ce sujet la page 5 de la note de 14 pages présentée par Cédric Villani à l’Office parlementaire d’évaluation des choix scientifiques et technologiques le 30 avril 2020)
- l’ensemble de la population est susceptible d’être contaminé. Dans le cas contraire (partie de la population vaccinée ou ne pouvant être rendue contagieuse par infection) il est possible d’introduire via Excel au moment opportun cette population dans le « compartiment R » sans passer par le « compartiment I » et de maintenir pour l’autre partie de la population un coefficient Reffectif égal à R0.
- les individus infectés ne sont pas systématiquement isolés de façon efficace. Dans certains pays, un individu détecté positif ou même ayant simplement eu un contact avec une personne infectée est systématiquement mis sans délai en quarantaine sévère, par exemple dans une chambre d’hôtel. Ce n’est pas le cas de la France (en dehors de quelques cas particuliers tels que l’équipage et les passagers de navires).
Compte tenu de ce qui précède et de la situation actuelle en France, dans la suite de cet article aucune distinction ne sera faite entre R0, Reffectif et R.
Les documents disponibles sur Internet donnent la courbe suivante pour l’évolution de Reffectif depuis le déconfinement de mai (avant le confinement R était d’environ 3 ; durant le confinement d’environ 0,7). À noter la baisse inexpliquée d’août‑septembre suivie de la remontée d’octobre.
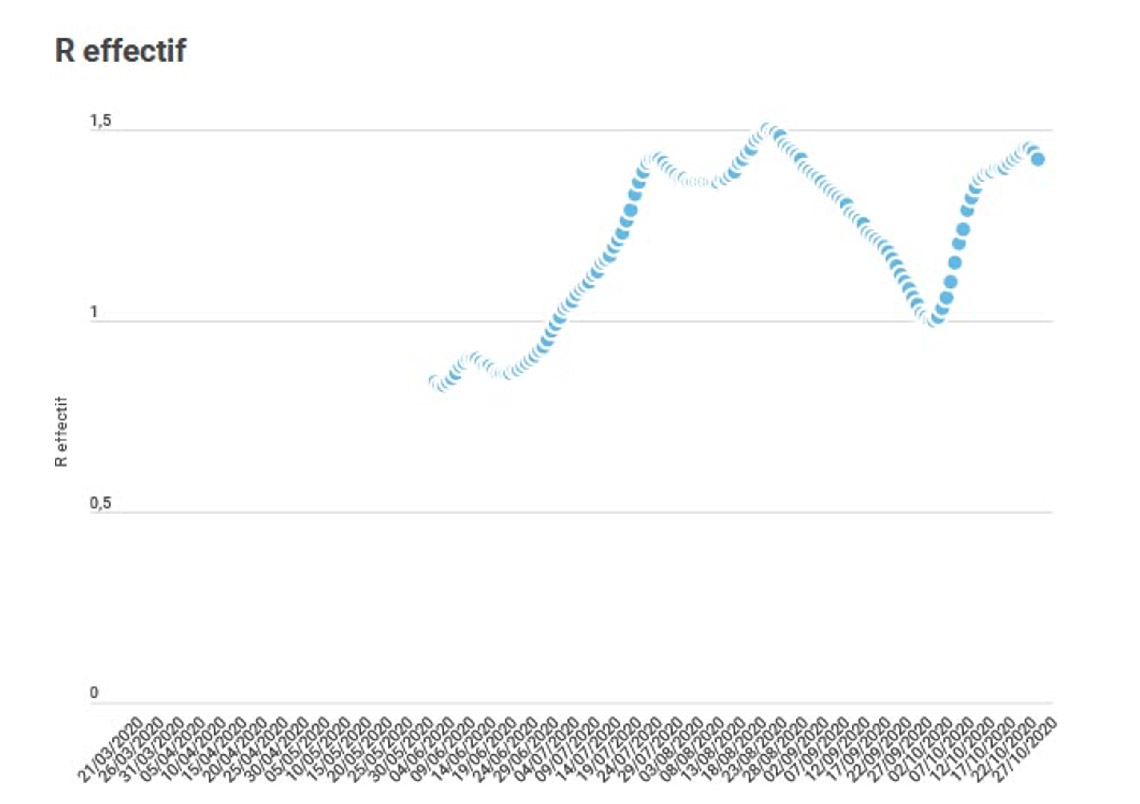
Conséquences sur le développement de l’épidémie
Modélisation utilisant Excel
(voir tableaux Excel en annexe 1)
Nous constatons que le Reffectif à la sortie du confinement est monté nettement plus haut que le 1,3 initialement prévu. Plusieurs causes sont possibles : brassage de population dû aux vacances d’été puis à la rentrée scolaire, volonté de retrouver rapidement une vie quasi-normale, sentiment d’absence de risque entretenu par certains membres du corps médical affirmant avec conviction que l’épidémie était terminée, ralliement à cette idée via les réseaux sociaux d’une frange importante de la population.
Si R restait après le 1er novembre au niveau 1,45 atteint vers la fin octobre 2020, l’utilisation des équations SIR de 1927 donnerait le diagramme suivant qui tient compte des variations de R constatées depuis mai 2020 :

Courbe marron : R x 10 000 000 – Courbe bleu foncé : nombre d’infectés simultané ( I ) – Courbe bleu clair : cumul des infectés guéris-immunisés et des décédés depuis le début de l’épidémie ( R )
On voit que ce diagramme rend bien compte du creux dans la courbe I représentant le nombre d’infectés simultanés pendant l’été 2020, suivi d’une remontée à partir de septembre. Néanmoins ces mouvements à la baisse puis à la hausse semblent timides par rapport à la réalité observée. Il paraît donc intéressant de voir si le modèle SIR bénéficiant de la correction (a priori relativement minime) proposée dans les articles de la J&R d’octobre donne une meilleure représentation de ce qui s’est passé jusqu’à maintenant.

Courbe marron : R x 10 000 000 – Courbe gris foncé : nombre d’infectés simultané ( I ) – Courbe bleu foncé : cumul des infectés guéris-immunisés et des décédés depuis le début de l’épidémie ( R )
Le remplacement dans Excel de
dR(t)/dt = γ I (t)
par
dR(t)/dt = – dS(t – D)/dt
ne pose aucune difficulté (voir annexe 1) et donne de façon inattendue pour le nombre d’infectés simultanés une forte accentuation de la baisse de l’été puis de la hausse de l’automne, nettement plus conformes à la réalité observée jusqu’à maintenant.
Pour le 1er semestre 2021 il indique, si R reste égal à 1,45, une hausse à la fois plus rapide et plus importante du nombre d’infections que le modèle SIR de 1927.
Cette propriété constatée empiriquement en utilisant Excel est confirmée par l’étude figurant dans le blog de David Madore (ancien de l’ENS Ulm, professeur de mathématiques à Télécom Paris) qui est arrivée à une conclusion semblable par une méthode différente en comparant les deux types de modélisation (effectuées à R constant) : SIR traditionnel (qu’il appelle « rétablissement en processus exponentiel ») et SIR modifié suivant la même correction que celle proposée dans l’article (« rétablissement en temps constant »). Les deux courbes qui suivent font apparaître ce que l’utilisation d’Excel avait permis de mettre en évidence : le changement d’équation n’est pas anodin et modifie de façon assez significative les courbes S (verte), I (rouge) et R (bleue), la courbe de variation de I étant plus « pointue ».


Conclusions – Perspectives
Si R reste à son niveau actuel, il existe un risque important de forte augmentation du nombre d’infectés pendant la fin de 2020 et la première moitié de 2021. Il semble donc vraisemblable que les pouvoirs publics chercheront dans l’immédiat à faire repasser R en-dessous de 1 « quoi qu’il en coûte ». Mais ceci ne règle pas le problème de façon définitive : les confinements ne peuvent pas être éternels …
Alors quelles sont les issues ?
Un miracle …
Pourraient survenir des mutations rendant la Covid-19 moins contagieuse ou moins virulente. On pourrait également découvrir qu’une partie importante de la population bénéficie d’une immunité naturelle… et tirer immédiatement des modèles épidémiologiques les conclusions permettant de guider une modification de la politique sanitaire.
La recherche de l’immunité collective
Si nous revenons à l’absence de contraintes du mode de vie que nous connaissions avant l’épidémie, le R0 Covid-19 correspondant est de l’ordre de 3. La courbe de l’annexe 2 montre qu’à ce niveau, les deux tiers de la population devront avoir été contaminés avant que l’épidémie commence à régresser. Mais ceci ne veut pas dire que l’épidémie cessera immédiatement : la période d’extinction fera passer le nombre total de personnes ayant été contaminées depuis le début de l’épidémie à près de 95 % de la population. À moins bien sûr qu’existe chez beaucoup de nos concitoyens l’hypothétique immunité naturelle évoquée plus haut.
Si on estime que le taux de létalité (nombre de décès / nombre total d’infectés) depuis le début de l’épidémie est de l’ordre de 0,5 à 1 % et que l’amélioration de la prise en charge des cas graves va permettre de le diviser par 2, ceci correspondrait à un total de 100 à 200 000 décès entre le début de l’épidémie et l’atteinte de l’immunité collective, suivis de 50 à 100 000 pendant la période d’extinction de l’épidémie qui suivrait. Une autre conséquence serait la submersion complète de notre système hospitalier.
Ni le gouvernement ni l’opinion publique ne sont prêts à laisser délibérément se développer une telle option basée sur la remontée à 3 du coefficient R.
Une navigation opportuniste permettant d’attendre l’arrivée d’un vaccin et/ou d’un remède
En dehors de l’éventuel miracle évoqué plus haut, ceci semble être la seule voie possible. Mais elle risque d’être de plus en plus mal accueillie par la population. Le retour périodique de périodes de confinement total ou de restrictions sévères aura un effet désespérant sur l’opinion publique et amènera vraisemblablement des réactions imprévisibles qui pourront être amalgamées avec d’autres types de mécontentements.
Enfin continueront à prospérer, transmises par les médias et les réseaux sociaux, des idées complotistes chez toute une frange de la population influencée par des membres du corps médical ayant bien compris que des prises de position à contrepied de la doxa officielle étaient la meilleure façon d’accéder à la notoriété.
Tout ceci risque d’entraîner le refus de la vaccination par une part importante de la population et d’induire un retard dans la disparition de l’épidémie ou même de la rendre chronique.
Annexe 1 : Modélisation utilisant Excel
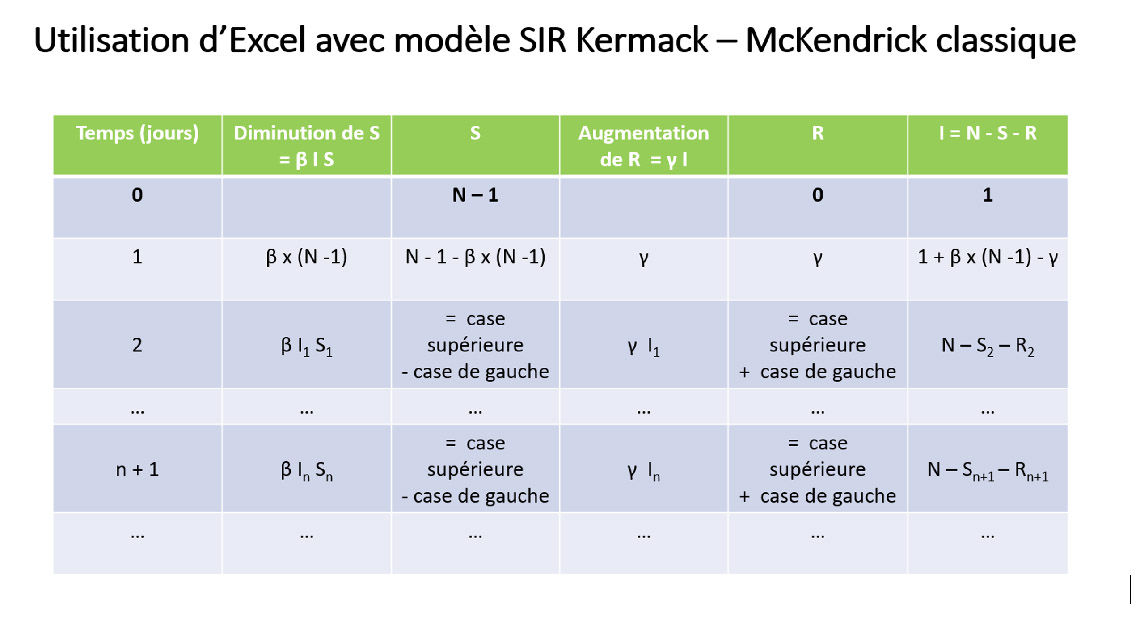

Annexe 2 : Précision sur le taux de contamination de la population apportant une immunité collective (herd immunity)
(cf. l’article « Une modélisation simple utilisant Excel … » dans la J&R n° 758 d’octobre 2020)
L’emploi d’Excel permet de déterminer facilement le taux d’immunité collective, c’est-à-dire le pourcentage de la population qui doit avoir été contaminé (ou vacciné, ou éventuellement ne pouvoir devenir contagieuse) pour que l’épidémie s’arrête d’elle-même. Il suffit de prolonger le tableau contenant S, I et R jusqu’à ce que I atteigne son maximum Imax.
On remarque que ce taux est très dépendant de R. Une série d’essais Excel avec des R allant de 1 à 4 donne la courbe suivante, qui est conforme avec la formule donnée dans les cours d’épidémiologie pour une épidémie à R constant :
Seuil d’immunité collective selon le modèle SIR de 1927 = 1 – 1/R.

N’est donc pas totalement exacte l’affirmation que l’on entend ou lit souvent, selon laquelle pour atteindre une immunité collective il faut que le taux total de personnes ayant été infectées dépasse 60 ou 70 %. Ceci n’est vrai si on souhaite simultanément permettre à la population de retrouver exactement le même mode de vie qu’avant l’épidémie (aucune restriction aux rencontres, aux déplacements, aucun port de masque, pas de gestes-barrières, pratique universelle des bises et des accolades …).
La courbe montre que si une population réussit à maintenir de façon durable un R inférieur à 1,5 l’immunité collective est obtenue dès que le cumul d’infectés atteint 33 % de la population (par exemple un peu plus de 20 % pour un R de 1,3). La combinaison d’un R et d’un taux cumulé d’infection de la population permettant de se positionner au-dessus de la courbe permet d’attendre l’arrivée d’un vaccin, d’un remède ou d’une éventuelle mutation favorable du virus. Certaines zones à forte densité de population sont vraisemblablement en train d’atteindre ce niveau, mais s’y maintenir de façon durable impose de ne pas laisser augmenter le R qui aura permis d’en bénéficier.
À noter qu’existe à la fin de l’article de la J&R n° 758 « Une modélisation simple utilisant Excel … » une erreur d’interprétation du terme « immunité collective » : traditionnellement son seuil correspond à l’atteinte du pic de l’épidémie – nombre maximum d’infectés simultanés ou Imax –, moment à partir duquel l’épidémie commence à régresser. Le schéma de l’article du n° 758 rend compte d’un pourcentage différent (et plus important) qui est celui du total de la population qui aura été contaminé à la fin de l’épidémie.
Pourcentage de la population ayant été contaminé en fin d’épidémie en fonction de R
Taux I final = Taux final d’infectés selon le modèle SIR de 1927
Taux I final = 1 – exp ( ‑R x Taux I final )

Les deux courbes sont différentes car l’épidémie continue après le pic de Imax jusqu’à son extinction totale, et il y a donc encore de nombreuses infections après l’atteinte du seuil d’immunité collective.
Le e = mc2 de l’épidémiologie
D’après le modèle SIR de 1927, dans une population non-vaccinée et sans aucune immunité naturelle,
tant que la proportion d’individus ayant été infectés est faible, à l’instant t
le nombre d’infectés croît (ou décroît) comme une fonction exponentielle d’exposant (R‑1) x t / D
R étant le « taux de reproduction » diffusé régulièrement
D la durée moyenne d’infection
Pour les non mathématiciens : exponentiel n’est pas systématiquement synonyme de croissance rapide
Si R est plus petit que 1, l’exposant est négatif et le nombre d’infectés décroît
Si R est très légèrement supérieur à 1, l’exposant est très petit et le nombre d’infectés croît lentement





Commentaire
Ajouter un commentaire
Commentaire de l’auteur. Désolé, mas 2 erreurs à rectifier dans l’article
1 – » Rappelons que R0 est égal au nombre quotidien de rencontres potentiellement contaminantes d’un infecté avec n’importe quel autre membre de la population multiplié par la proportion de ces rencontres débouchant sur une infection réelle puis divisé par le nombre moyen de jours entre infection et guérison ou décès « . Il faut lire » divisé par γ qui est l’inverse du nombre moyen de jours entre infection et guérison ou décès » ou « multiplié par par le nombre moyen de jours entre infection et guérison ou décès »
2 – » Reffectif (nombre de reproduction effectif) est égal à R0 à deux conditions :
J’ai été induit en erreur par la page 5 de la note de 14 pages présentée par Cédric Villani à l’Office parlementaire d’évaluation des choix scientifiques et technologiques le 30 avril 2020 qui indiquait que Reffectif est égal à m x (1‑p) x R0, m étant la proportion de la population susceptible d’être contaminée. J’ai pensé que la population non contaminable dont il parlait était uniquement celle qui bénéficiait d’une éventuelle immunité naturelle ou par vaccination. En fait il parlait de la proportion de la population qui n’avait pas été immunisée par l’épidémie elle-même. La formule correcte est donc : Reffectif = R0 x S(t) x (1‑p) / N.
Ceci n’a pas beaucoup d’importance tant que la proportion de la population infectée puis guérie ou décédée n’est pas importante, puisqu’alors S(t) est proche de N. Cette mise au point n’a pas de conséquence sur la suite de l’article, mais bien évidemment la phrase « Compte tenu de ce qui précède et de la situation actuelle en France, dans la suite de cet article aucune distinction ne sera faite entre R0, Reffectif et R » est inexacte.