Principe de précaution et évaluation des risques : la nouvelle doctrine de sécurité sanitaire

Un contexte nouveau
Le défi des crises de sécurité sanitaire
La société française, comme toutes les société développées, connaît depuis quelques années une succession de crises touchant à la sécurité sanitaire. Pour ne s’en tenir qu’aux crises majeures, l’affaire du sang contaminé a posé le problème de la sécurité des produits thérapeutiques, celle de la vache folle celui de la sécurité alimentaire et celle de l’amiante celui de la sécurité des substances chimiques.
Ces différentes crises traduisent l’émergence de problèmes nouveaux mais aussi d’une approche nouvelle des questions de sécurité sanitaire, ce que traduit la référence au principe de précaution. Elles ont révélé l’inadéquation du système actuel de sécurité sanitaire au regard de ces nouvelles exigences et mis à l’ordre du jour la refonte de celui-ci. Cette exigence a conduit aussi à inventer des outils scientifiques pour évaluer les risques pour la santé liés aux facteurs physiques d’environnement.
Le poids croissant des pathologies chroniques
L’amiante illustre le coût sanitaire d’un facteur d’environnement mal évalué a priori et même a posteriori, une fois les premières données épidémiologiques publiées. Il n’est vraisemblablement pas le seul. Même si on est encore très loin de connaître l’ensemble de la relation santé/environnement notamment pour ce qui est des cancers, ce lien apparaît très important au vu de l’évolution des causes de mortalité et de morbidité. Aux États-Unis, les principales causes de mortalité en 1900 étaient dues aux maladies infectieuses (31,9 %), au premier rang desquelles la tuberculose. Les cancers ne représentaient que 3,7 % des causes de mortalité. Aujourd’hui, les maladies infectieuses ont globalement régressé (4,9 %) et les maladies chroniques (maladies cardiovasculaires et cancers) sont devenues prédominantes (33,2 % et 23,8 % des décès).
En France, l’évolution a été de même nature. Le cancer est la première cause de mortalité chez l’homme avec 32 % des causes de décès. C’est devenu la première cause de mortalité avant 65 ans, avec 36 % des causes de décès (HCSP, 1996). La croissance des cancers n’est pas simplement due à un effet mécanique lié à la diminution des autres causes de mortalité ou à l’allongement de la durée de la vie. L’incidence, en données corrigées sur l’âge, a progressé régulièrement en France depuis vingt ans, de l’ordre de 1 % par an. Aujourd’hui, le cancer touche un homme sur deux et une femme sur trois. Certaines tumeurs ont connu une croissance spectaculaire : prostate + 218 %, cerveau + 80 %, sein + 60 %…
La croissance de l’incidence des cancers de l’enfant dans tous les pays du monde (particulièrement leucémies et tumeurs du cerveau), alors que la mortalité diminue en raison des progrès thérapeutiques, est une autre indication que le vieillissement de la population n’est pas la seule explication de la progression des cancers. Une évolution aussi rapide sur des périodes de temps aussi courtes que deux décennies plaide pour l’existence d’une responsabilité significative des facteurs de risque environnementaux dans la genèse des cancers. Ceux-ci ne peuvent être limités aux seuls tabagisme et alcoolisme, lesquels sont par ailleurs en diminution, même si ces derniers restent des causes importantes (HCSP, 1996).
L’étude des populations migrantes montre que d’une façon très générale celles-ci acquièrent le profil de cancers du pays d’accueil. Par exemple, les Japonaises émigrées à Hawaii ont un taux de cancer du sein quatre fois plus élevé que celui des Japonaises vivant au Japon, celui des Américaines d’origine européenne étant six fois plus élevé que celui de ces dernières. À l’inverse, le taux de cancer de l’estomac diminue d’un facteur 4. Le NIEHS (National Institute of Environmental Health Sciences) aux États-Unis estime que 70 à 80 % des cancers sont liés à l’environnement, l’environnement étant compris au sens large, c’est-à-dire incluant l’exposition via le mode de vie, le travail, l’alimentation ou l’environnement stricto sensu (1992).
Les cancers représentent la préoccupation la plus grave en termes de santé publique, mais ce n’est pas le seul groupe de pathologies dont il apparaît qu’elles sont liées à des facteurs de risque environnementaux. Sont considérées comme très liées à l’environnement les pathologies affectant le système respiratoire (l’asthme a doublé en dix ans pour les moins de 18 ans au cours des dix dernières années), le système immunitaire (croissance des allergies), le système nerveux (développement des maladies neurodégénératives comme la maladie d’Alzheimer ou la maladie de Parkinson), la reproduction (interrogation sur la diminution de la qualité du sperme au cours des vingt à cinquante dernières années et sur la croissance de l’infertilité qui affecte environ 15 % de la population), la santé de l’enfant (l’enfant apparaît plus sensible à l’action de facteurs de risque environnementaux en raison de caractéristiques tenant à sa physiologie et à son activité) (Baldwin, 1996).
Pour le département de la santé des États-Unis, les causes de mortalité prématurée sont liées pour 20 % à l’environnement, 50 % au mode de vie, 10 % au système de santé et 20 % à des causes génétiques (Paxman, 1997).
Ceci donne un ordre de grandeur suffisamment important pour considérer qu’une politique de santé moderne ne peut plus se concevoir sur le seul schéma d’amélioration des techniques de soin ou des conditions d’accès au soin pour améliorer l’état de santé des populations et qu’elle doit prendre en compte l’action sur les facteurs de risque environnementaux. C’est ce que traduit la notion de santé environnementale.
Le principe de précaution
Ewald (1993) considère trois périodes dans le rapport au risque. La première période naît au XIXe siècle et correspond à l’âge de la prévoyance. Elle vise à se prémunir contre les conséquences du risque, faute de pouvoir agir sur des causes que l’on identifie mal. La seconde période correspond à l’âge de la prévention. La prévention est différente de la prévoyance en ce sens qu’elle ne vise pas la compensation des dommages, mais à en réduire l’éventualité. La logique de prévention se construit autour de facteurs de risque clairement identifiés et dont la relation avec la pathologie qu’ils induisent est univoque, sur la base du modèle infectieux (un micro-organisme = une pathologie). Cette logique ne prend pas en compte les situations d’incertitude ou de relation multifactorielle.
C’est cette distance entre capacités techniques et possibilité de leur maîtrise qui donne naissance au principe de précaution. La précaution ne s’inscrit pas dans la continuité de la prévention. La prévention suppose la connaissance. On ne peut prévenir que ce que l’on connaît. La précaution oblige, par contre, à prendre en compte des risques non ou mal connus.
Le principe de précaution est devenu un principe de droit international à l’occasion de la conférence de Rio sur la protection de l’environnement organisée sous l’égide des Nations Unies en 1992.
La déclaration finale affirme que « en cas de risque de dommages graves ou irréversibles, l’absence de certitude scientifique absolue ne doit pas servir de prétexte à remettre à plus tard l’adoption de mesures effectives visant à prévenir la dégradation de l’environnement ».
Le traité de Maastricht (article 130 R relatif à l’environnement) a précisé que ce principe s’appliquait aussi à la « protection de la santé des personnes ».
L’évaluation des risques
La sécurité sanitaire des substances chimiques représente un élément essentiel d’une politique de santé environnementale. C’est « un défi global à l’échelle mondiale » selon le directeur du programme international conduit sous l’égide de l’OMS (Mercier, 1995). Des études récentes montrent en effet un déficit de connaissances de base sur les effets toxiques y compris pour les substances les plus utilisées.
On ne dispose de données complètes pour les HPV (High Production Volume) que dans 7 % des cas (Betts, 1998). Lorsque ces données existent, il est nécessaire de se doter d’une méthodologie pour les analyser, c’est ce besoin qui a donné naissance à l’évaluation des risques.
L’acte de naissance officielle de celle-ci est le rapport du Conseil national de la recherche de l’Académie des sciences des États-Unis adopté en 1983 et reconfirmé en 1994. Celui a été adopté depuis dans le monde entier et notamment au niveau européen à l’occasion des règlements et directives publiés en 1993 et 1994 par l’Union européenne pour l’évaluation des substances nouvelles et existantes.
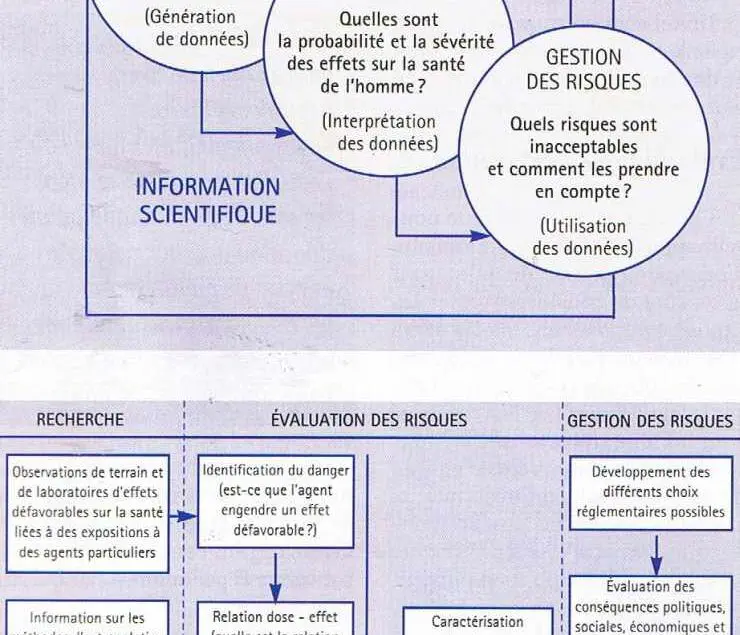
Ce paradigme repose sur deux assertions fondamentales illustrées par les figures ci-après (Académie des sciences des USA) :
- le processus d’évaluation et de gestion du risque se décompose en trois phases successives.
La recherche et l’évaluation des risques sont du domaine scientifique. La gestion des risques est du domaine politique.
- l’évaluation des risques se décompose elle-même en quatre phases : identification des dangers, relation dose-effet, évaluation de l’exposition et caractérisation des risques.
Les notions de danger et de risque, souvent confondues dans le langage courant, sont clairement distinguées.
L’évaluation des risques apparaît ainsi comme le corollaire scientifico-technique du principe de précaution.
Le danger évoque le caractère intrinsèque d’une substance, alors que la notion de risque évoque la probabilité d’occurrence d’un dommage occasionné par le potentiel dangereux de la substance. C’est la nature de l’exposition qui détermine le risque lié à une substance dangereuse.
Il ne s’agit plus d’agir une fois les dommages sur la santé dûment constatés, mais d’anticiper les effets sur la santé de l’homme en utilisant un cadre méthodologique utilisant les meilleures connaissances scientifiques disponibles.
Substances avec seuil d’effet
La caractérisation des risques est différente selon que l’effet est de type déterministe (effet systémique avec un seuil d’effet) ou de type probabiliste (effet cancérogène sans seuil d’effet).
Dans le premier cas, on détermine le seuil d’effet à partir des données expérimentales obtenues chez l’animai, en appliquant des facteurs de sécurité. Les données animales fournissent une DSENO (Dose sans effet nocif observé) ou une DMENO (Dose minimale induisant un effet nocif observé) (NOAEL et LOAEL des Anglo-Saxons). L’OMS (1994) préconise de re tenir comme facteurs de sécurité :
- un facteur de 1 à 10 pour extrapoler de l’animal à l’homme,
– un facteur de 1 à 10 pour tenir compte des susceptibilités au sein de l’espèce humaine,
– un facteur supplémentaire de 10 peut être retenu pour certains types d’effet comme les effets de type tératogène (induction de malformation sur la descendance),
– un facteur supplémentaire pouvant aller jusqu’à 10 peut être retenu si les données expérimentales fournissent une DMENO et non une DSENO, ou encore si la qualité des données est jugée insuffisante.
Ces facteurs sont encore largement empiriques. Le choix de facteurs de sécurité étant fait, on détermine ainsi une dose de référence. Cette dose est considérée comme le seuil d’effet toxique de la substance considérée chez l’homme. Le risque pour une population est alors évalué en fonction de la proportion de cette population susceptible d’être exposée à un niveau supérieur à cette dose.
Le choix de la période d’exposition varie selon la nature de l’effet toxique. Par exemple, pour les effets sur le développement embryo-fœtal, on considère qu’une dose unique est suffisante pour induire des effets nocifs si elle est appliquée à une période sensible de la gestation (EPA, 1991).
Substances sans effet de seuil
Pour les substances sans effet de seuil, c’est-à-dire les substances cancérogènes, on détermine à partir des données expérimentales ou à partir des données épidémiologiques, généralement obtenues en milieu professionnel, un ERU (Excès de risque unitaire). Cet ERU correspond à l’excès de décès attendus dans une population exposée sur une vie entière (estimée à 70 ans) pour une pathologie donnée à la suite d’une exposition unitaire (par exemple, une concentration atmosphérique de 1 µg/m3). L’extrapolation se fait le plus souvent selon le modèle d’extrapolation dit « linéaire sans seuil ».
Le choix d’un risque acceptable n’est pas un choix de nature scientifique, c’est un choix politique et sociétal.
Ce modèle est considéré comme le plus vraisemblable. C’est aussi le plus protecteur de la santé humaine et il est donc souvent retenu en vertu du principe de précaution. Par exemple, l’OMS (1997) a retenu, sur la base de données épidémiologiques en milieu professionnel, pour le benzène un ERU de 6 x 10-6 / (µg/m3). Cela signifie qu’une exposition de 1 million de personnes, pendant soixante-dix ans, à une concentration de 1 µg/m3 de benzène est susceptible d’induire six cas de décès supplémentaires par leucémie pendant la même période.
Ce modèle d’extrapolation sans seuil induit la notion de risque acceptable, car le risque zéro n’existant pas, il est nécessaire pour déterminer une valeur limite environnementale de faire le choix d’un risque acceptable. Aux États-Unis, le risque acceptable retenu au niveau populationnel est de 10-6. L’OMS a retenu pour ses recommandations de valeurs limites dans l’eau le risque de 10-5. C’est sur la base de ce niveau de risque qu’a été retenu en France un objectif de qualité pour le benzène de 2 µg/m3 (Décret du 6 mai 1998).
Un tel choix n’est possible qu’au vu de la mise en évidence des coûts et des bénéfices, du point de vue tant sanitaire qu’économique.
Évaluation de l’exposition
On voit que, au vu de cette nouvelle appréciation du risque sanitaire d’origine environnementale, il est nécessaire de considérer toutes les expositions possibles, via les différents milieux, l’air, l’eau, l’alimentation, les sols, que l’exposition se fasse sur le lieu de travail, le lieu d’habitation ou à l’extérieur des locaux. L’individu accumule un certain nombre d’expositions via les différents milieux et c’est la dose totale ainsi accumulée qui permet d’évaluer le risque. L’évaluation de l’exposition provient de mesures faites sur les individus, mais le plus souvent faute de ce type de données, on utilise des scénarios vraisemblables pour calculer des doses d’exposition. Pour évaluer les risques liés aux sols, on utilisera par exemple des scénarios intégrant le temps de séjour, mais aussi une éventuelle consommation des légumes produits dans le potager. Si l’on évalue, par exemple, le coût sanitaire de l’exposition au benzène, il est nécessaire de considérer l’exposition qui est la résultante de l’exposition via l’air extérieur mais aussi via l’air intérieur.
L’évaluation des risques permet ainsi de fixer des valeurs limites environnementales dans l’air, l’eau, l’alimentation ou dans les sols. Cette méthode permet donc une approche globale et donc de hiérarchiser les risques afin de déterminer ensuite des priorités d’action sur les milieux prioritaires.
Si l’on considère l’exposition liée au mercure, il est nécessaire d’évaluer l’exposition dans tous les milieux, car le mercure se trouve dans l’air, l’eau, l’alimentation et dans les produits de santé comme les amalgames dentaires. L’EPA a proposé récemment de fixer une dose de référence de 0,1µg/kg/j en méthylmercure (MeHg) dans le poisson. MeHg est le composé du mercure agissant aux plus faibles doses. L’effet critique est de type neurotoxique chez l’enfant. Ceci se fonde sur des données épidémiologiques obtenues aux îles Féroé montrant un développement cognitif diminué chez des enfants de 7 ans dont les mères avaient à la naissance un taux d’imprégnation plus élevé en méthylmercure lié à la consommation de mammifères marins.
Dans le cas du mercure, la priorité d’action se situe plus au niveau de l’alimentation en poisson qu’au niveau de l’air. Pour le benzène, c’est par contre la pollution de l’air qui est déterminante.
Risque individuel et groupes sensibles
Un autre critère de jugement est celui du risque individuel. L’EPA retient un risque de 10-4. Cela signifie qu’un individu ne peut être exposé sur une vie entière à une probabilité sur 104 de décéder de son exposition environnementale. À titre de comparaison, le risque accident de la route est 10-2 (un citoyen français a une probabilité sur 100 de décéder au cours de sa vie dans un accident de la route).
Cette approche amène à étudier la distribution de probabilité au sein de la population générale et à se préoccuper des sous-groupes qui peuvent être plus particulièrement sensibles aux effets d’un toxique, en raison :
- d’un mode de consommation particulier (minorités ethniques, consommateurs de poissons, dans le cas des pollutions par le mercure ou les PCB par exemple…) ;
- de leur âge : les enfants ont une activité physique proportionnellement plus élevée que celle des adultes et donc, à poids égal, respirent plus de polluants. Ils ingèrent plus de fruits et de légumes et donc de résidus phytosanitaires que ces derniers (7 fois plus à poids égal). C’est ce qui a conduit l’EPA à retenir récemment un facteur de sécurité supplémentaire de 10 pour l’enfant ;
- de leur état de santé : asthmatiques, personnes âgées ou tout groupe de population présentant une particularité physiologique du type déficience enzymatique.
Une méthodologie de référence
L’évaluation des risques pour la santé et pour l’environnement est donc devenue aujourd’hui la méthodologie de référence au niveau international. Les modalités d’application peuvent cependant changer selon les pays et les organismes, même si les principes généraux sont les mêmes pour tous. L’OMS a publié sa propre grille d’analyse en 1994. Aux États-Unis, les lignes directrices de référence sont celles publiées par l’US EPA. L’Union européenne a publié en 1994 un guide technique en support de la directive 93/67/CEE pour les substances nouvelles et du règlement 1488/94/CE pour les substances existantes. Ce document comprend quatre volumes traitant :
1) de l’évaluation des risques pour la santé humaine,
2) de l’évaluation des risques pour l’environnement,
3) de l’utilisation des QSAR (relation structure-activité),
4) des scénarios relatifs aux émissions.
Conclusion
Une nouvelle doctrine de sécurité sanitaire a été mise en place au cours des dernières années. Fondée sur le principe de précaution et l’évaluation des risques pour la santé, elle est aujourd’hui partie intégrante de la réglementation française et européenne. Elle offre un outil permettant d’anticiper les effets sur la santé des substances chimiques.
La limite de la démarche tient à l’absence de données expérimentales pour un grand nombre de substances (on connaît en plus très peu de choses sur les effets d’une exposition cumulée aux toxiques ou aux autres nuisances) mais aussi au faible développement, notamment en France, des disciplines scientifiques de base : l’épidémiologie (relation entre état de santé et facteurs d’exposition), la toxicologie (étude de l’action des substances toxiques sur les organismes vivants) et l’expologie (étude de l’exposition des populations aux facteurs de risques environnementaux).
C’est donc un vaste chantier qui est ainsi ouvert.
On peut parler comme Paxman d’une deuxième révolution de santé publique (1997) de la même ampleur que celui de la première révolution de santé publique, celle qui s’est déroulée au début de ce siècle et a pu faire reculer les pathologies infectieuses par une action qui portait déjà sur l’environnement (adduction d’eau, assainissement, amélioration de l’habitat).