L’industrie du dispositif médical dans le monde


L’industrie du dispositif médical est une industrie complexe et hétérogène. C’est la loi du 18 janvier 1994 qui introduit dans le droit français la définition du dispositif médical (article L. 665–3 du Code de la santé publique).
On entend par dispositif médical tout instrument, appareil, équipement, matière, produit, à l’exception des produits d’origine humaine, ou autre article utilisé seul ou en association, y compris les accessoires et logiciels intervenant dans son fonctionnement, destiné par le fabricant à être utilisé chez l’homme à des fins médicales et dont l’action principale voulue n’est pas obtenue par des moyens pharmacologiques ou immunologiques ni par métabolisme, mais dont la fonction peut être assistée par de tels moyens. Les dispositifs médicaux qui sont conçus pour être implantés en totalité ou en partie dans le corps humain ou placés dans un orifice naturel, et qui dépendent pour leur bon fonctionnement d’une source d’énergie électrique ou de toute source d’énergie autre que celle qui est générée directement par le corps humain ou la pesanteur, sont dénommés dispositifs médicaux implantables actifs.
L’industrie du dispositif médical comprend par exemple les matériels d’imagerie médicale, les pansements utilisés dans les salles opératoires, mais aussi les prothèses externes utilisées par les orthopédistes, les prothèses internes telles que les valves cardiaques, les matériaux de perfusion ou de distribution des fluides. Il y a plus de 3 000 familles de produits différentes représentant environ 84 000 produits en tout.
Le tableau I illustre cette diversité.
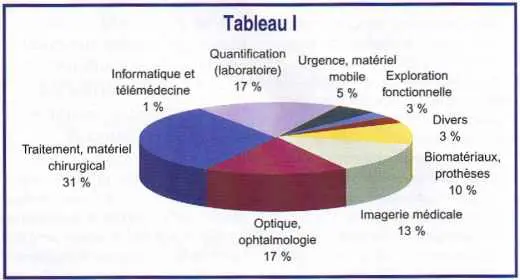
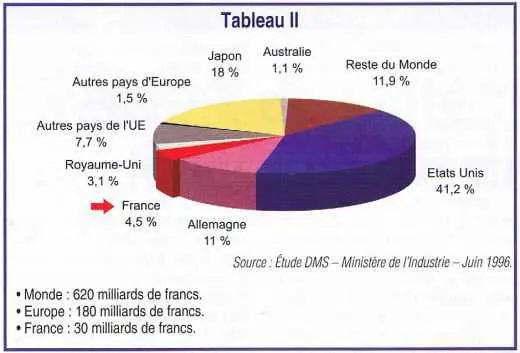
La complexité des domaines couverts par l’industrie des dispositifs médicaux, la multiplicité des secteurs et l’absence de nomenclature internationale des produits rendent la collecte des statistiques difficile et leur comparaison aléatoire. Le tableau II illustre la répartition géographique de cette industrie.
Enfin les prix de ces produits sont très variables, de quelques centimes à 20 millions de francs. En France, l’industrie des technologies médicales représente un secteur de poids avec un chiffre d’affaires d’environ 30 milliards, employant 20 000 personnes et réalisant 25 % à l’export.
Avant sa mise sur le marché, tout dispositif médical doit obtenir le marquage CE (Conformité européenne). Ce marquage CE est délivré par un organisme notifié (autorité nationale d’un État membre de l’EU) qui évalue la conformité du dispositif médical en matière de sécurité et de santé par rapport aux textes de la directive européenne dont il dépend (93÷42, 98⁄79, ou 90⁄385). Une fois que le produit a reçu le marquage CE, il peut être vendu librement dans tous les États membres de l’Union européenne sans autre vérification ou modification.
Des compétences et des métiers multiples
L’industrie du dispositif médical est une industrie qui comporte une forte présence d’ingénieurs. Toutes les technologies sont mises en œuvre, mécanique, électricité, électronique, informatique, textile, chimie… Plus de 50 disciplines telles que, par exemple, la physique des solides ou l’holographie sont présentes dans l’industrie du dispositif médical. Plus de 50 spécialités médicales telles que la chirurgie orthopédique, la cardiologie, l’ophtalmologie ou la néphrologie utilisent les produits et systèmes de l’industrie du dispositif médical.
Celle-ci développe, fabrique et conditionne des produits à l’attention des médecins, chirurgiens et des professions paramédicales, afin que, à leur tour, ils en fassent bénéficier le patient. On comprend, par exemple, que ce ne peut être le malade lui- même qui achète sa prothèse de hanche et donc le risque inhérent à l’acte chirurgical engage la responsabilité du chirurgien avant celle du fabricant du dispositif.
Les dispositifs implantables nécessitent une adaptation au patient. De ce fait cet aspect doit être intégré lors des phases de recherche et développement. Cela est évident pour les prothèses externes, telles les jambes ou les mains articulées qui s’adaptent aux activités des patients en fonction de l’âge, de l’activité, de la pratique éventuelle d’un sport, mais s’applique aussi dans le cas de prothèses internes (valves cardiaques, défibrillateurs implantables ou cœur artificiel).
En complément des produits, l’industrie du dispositif médical fournit à ses clients des services en rapport avec l’exploitation du dispositif, tels que la formation à l’utilisation pratique, un service d’assistance technique disponible vingt-quatre heures sur vingt-quatre, des compétences en matière de gestion du parc de matériel ou en matière de logistique pour la livraison des patients à domicile, par exemple.
Baxter est une société américaine dont la moitié du chiffre d’affaires (6 milliards de dollars) est réalisée dans le dispositif médical. L’entreprise est présente dans plus de 100 pays et comporte 175 sites de production. 40 000 personnes travaillent dans les différents domaines d’activité du groupe : la transfusion sanguine, les médicaments dérivés du sang et les vaccins, l’administration des médicaments (systèmes de perfusion, pompes et diffuseurs portables), la nutrition parentérale, les gaz anesthésiques et les produits destinés aux traitements de l’insuffisance rénale chronique terminale.
L’association des technologies
Dans l’industrie du dispositif médical, la recherche proprement dite, c’est-à-dire fondamentale, est peu réalisée par l’entreprise et c’est plutôt le développement au sens anglo-saxon du terme (development = mise au point) qui draine la majorité des investissements. En matière de recherche, ce sont essentiellement des contrats de collaboration qui sont mis en place avec des structures publiques.
Dans le développement de nouveaux produits, Baxter dépense environ 1 million de dollars en R & D par jour, ce qui représente environ 6 % du chiffre d’affaires, et s’intéresse à des disciplines très diverses. Nous allons illustrer la pluridisciplinarité des connaissances nécessaires à ces développements, à partir de domaines dans lesquels Baxter est présent.
Dans le cadre de l’amélioration de l’administration des médicaments, il existe depuis quelques années des domaines de recherche sur les injections transdermiques à base de micro-aiguilles. Comparable au patch, simple à utiliser, cette technique permettrait aussi d’administrer des médicaments qui sont habituellement injectés par une seringue.
Ces microaiguilles, traversant l’épiderme, permettraient d’injecter une grande variétés de molécules. N’atteignant pas les terminaisons nerveuses du derme elles seraient indolores. La capacité de ces microaiguilles à diffuser sur des tissus de peau de grosses protéines telles que la sérum albumine est à l’étude.
C’est une technique classique de microélectronique, la pulvérisation ionique réactive, qui permet de fabriquer un réseau de microaiguilles en silicium : un carré de 3 mm de côté, hérissé de 400 microaiguilles longues de 150 micromètres et pas plus épaisses qu’un cheveu. Le procédé consiste à arracher des atomes à une cible (ici en silicium) sous l’effet d’un faisceau d’ions (fluorine et oxygène dans ce cas) avec lesquels elle est particulièrement réactive. Un masque en résine permet d’opérer une sorte d’usinage à l’échelle atomique. La technique est couramment utilisée pour l’impression des circuits intégrés, mais pour des épaisseurs bien moindres.
Si ce système fait ses preuves on pourrait alors imaginer de graver un microprocesseur en même temps que les microaiguilles pour disposer d’un système programmable de délivrance de médicaments, par exemple chez les diabétiques pour contrôler l’injection d’insuline en fonction de leur glycémie.
Toujours dans le domaine du traitement du diabète, nous pouvons mentionner les pompes à insuline implantables. Trois éléments constituent le système d’infusion continue (sur plusieurs jours) d’insuline. Un boîtier en titane en forme de disque implanté dans le tissu abdominal sous-cutané comprend le réservoir d’insuline, un système de piston, un réservoir électronique et une pile au lithium.
Un système télémétrique permet au patient ou au médecin de programmer la pompe, ou d’ajuster le débit d’infusion. De nombreux travaux sont actuellement en cours pour améliorer la biocompatibilité de ces systèmes et reproduire au mieux le fonctionnement physiologique du pancréas.
L’insuffisance rénale chronique terminale touche actuellement environ 35 000 personnes en France. Les patients atteints de cette maladie peuvent être traités, en dehors de la greffe rénale, par deux techniques de suppléance, l’hémodialyse ou la dialyse péritonéale. Ces techniques peuvent être mises en place soit dans un cadre hospitalier soit à domicile.
Majoritairement, les patients atteints de maladies chroniques souhaitent un retour au domicile dès que possible. Aujourd’hui, il existe encore des barrières techniques pour exaucer ces souhaits. La télémédecine pourrait apporter, dans certains cas, une solution à ces problèmes.
La télémédecine c’est l’utilisation des télécommunications et de l’informatique dans la pratique et la formation médicale. Des médecins effectuent des consultations à distance (téléconsultation), interprètent des images médicales à distance (téléexpertise), ou encore des patients sont surveillés à domicile plutôt qu’à l’hôpital (télésurveillance).
La télémédecine nécessite une collaboration entre informaticiens, industriels du dispositif médical susceptibles de transmettre les informations médicales utiles au médecin (pouls, pression artérielle, surveillance visuelle du cathéter de dialyse péritonéale par exemple), industriels des télécommunications (transmission en continu et immédiate de grandes quantités d’informations), médecins, économistes (évaluation du rapport coût/efficacité de la technique).
Les biotechnologies font aussi partie du monde des dispositifs médicaux. De nombreux patients atteints de cancer sont traités par chimiothérapie afin de détruire les cellules tumorales. L’un des obstacles à l’efficacité du traitement réside dans l’acquisition, par ces cellules, de résistances aux antimitotiques. Différentes stratégies ont été proposées pour tenter de s’opposer à ces résistances. En particulier, l’augmentation des doses de chimiothérapie paraît capable, dans un certain nombre de cas, d’annuler les mécanismes de protection mis en œuvre par la cellule.
Introduite au début des années 1980, la chimiothérapie à hautes doses avec autogreffe de moelle osseuse (ou, à l’heure actuelle, autogreffe de cellules souches hématopoïétiques) a dans ce domaine constitué un des espoirs de ces dernières années. Les cellules souches, ou indifférenciées, du sang ont toujours été considérées comme » le Saint-Graal de l’hématologie et de l’immunologie « .
Ces cellules, créées par la moelle osseuse, sont les seules à posséder deux capacités : se différencier en n’importe quelle cellule du sang (globules rouges et blancs, plaquettes) et se renouveler en nouvelles cellules souches. Le problème est qu’elles sont très rares – une sur 100 000 cellules de la moelle – et qu’elles sont très difficiles à distinguer d’autres cellules qui en sont à un stade plus avancé de la différenciation. Elles ont maintenant été trouvées et isolées grâce à l’identification d’un marqueur particulier, l’antigène de surface CD34 exprimé au niveau d’une sous-population de cellules.
Malgré cette limitation, la glycoprotéine CD34 est devenue le marqueur de choix dans la purification de cellules souches. Actuellement tous les protocoles expérimentaux et cliniques sont en effet ciblés sur la population cellulaire CD34+ (quantification ou purification). Différents dispositifs médicaux de purification ont été employés, basés sur des différences de densité, d’expression d’antigènes, de niveau du cycle cellulaire, et d’activation pour l’obtention des cellules souches.
Conclusion
La pluridisciplinarité des sciences, des techniques et des métiers se développe à grande vitesse dans le domaine des sciences de la vie et favorise l’innovation. Pour mettre en œuvre les thérapies et pratiques cliniques nouvelles, l’industrie du médicament et l’industrie des dispositifs médicaux travailleront de plus en plus en commun.
À titre d’exemple, les stents1 extensibles sont largement utilisés au cours des procédures d’angioplastie coronaire2. Un sérieux problème réside dans la survenue d’une réobstruction progressive. Aujourd’hui est à l’étude un stent coronaire original recouvert d’un polymère porteur d’un plasmide à ADN, qui permet une libération locale d’un produit luttant contre la réobstruction tout en permettant l’extension et le déploiement du stent. La mise au point de ce principe pose de nombreux défis, notamment en ce qui concerne la surface très réduite du stent et la nécessité du maintien de sa fonctionnalité avec un revêtement polymérique circonférentiel.
Indispensable au progrès des pratiques médicales, l’industrie du dispositif médical est aussi créatrice d’amélioration de la qualité de vie des patients tout en respectant un coût acceptable pour la collectivité. Son développement passe par une ouverture et une collaboration avec de nombreuses disciplines.
__________________________________
1. L’endoprothèse coronaire ou stent est définie comme un cylindre métallique à mailles plus ou moins lâches, destiné à être encastré dans la paroi artérielle. Ces treillis métalliques exercent une force radiale qui permet de maintenir, après angioplastie, le calibre artériel à une valeur prédéterminée.
L’action essentielle du stent est d’éviter le retour élastique de la paroi.
2. L’objectif de l’angioplastie est de dilater (en cas de sténose) ou de reperméabiliser (en cas d’occlusion) la lumière artérielle pour restituer un flux sanguin satisfaisant.

