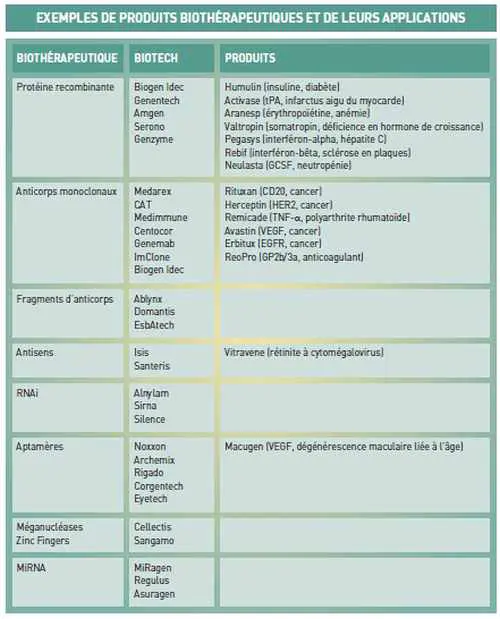
La course à la prochaine génération de biothérapeutiques


Anticorps, protéines recombinantes, antisens, aptamères, les générations de biothérapeutiques se succèdent au rythme des avancées scientifiques. Chaque génération donne lieu à un ballet au sein de l’industrie pharmaceutique, où chaque compagnie prend position par acquisition ou partenariat dans le but de dominer les approches biothérapeutiques qui feront les médicaments de demain.
La plupart des médicaments mis sur le marché au XXe siècle étaient de petites molécules, parfois substances naturelles mais plus généralement produites par synthèse organique. À partir des années quatre-vingt, les progrès de la biologie moléculaire ont permis de réaliser l’intérêt que pourraient présenter les biomacromolécules, en particulier les protéines, mais aussi des acides nucléiques, en tant que médicaments.
Ces produits, que l’on qualifiera de biothérapeutiques, sont l’objet d’efforts très intenses au niveau de la recherche et d’un intérêt important de la part des industriels, qui se traduit par des investissements conséquents. Quelles sont la situation présente dans le domaine des biothérapeutiques et l’approche stratégique de l’industrie pharmaceutique ?
Repères
Outre l’insuline, d’autres protéines recombinantes ont fait la preuve d’un intérêt thérapeutique, en particulier les hormones de croissance. L’administration de ces protéines permet de restaurer une fonction qui est absente ou mal réalisée chez le patient.
Protéines et anticorps
La production d’une protéine peut poser des problèmes de stabilité ou de solubilité
L’idée d’utiliser des protéines pour soigner une maladie est assez ancienne : depuis les années vingt, on administre à des patients diabétiques l’insuline qui leur fait défaut. Cette insuline est extraite de pancréas d’animaux. Grâce au génie génétique, on a pu depuis lors produire, dans des conditions de sécurité nettement améliorées, plusieurs types d’insuline recombinante, certaines possédant des propriétés intéressantes, par exemple l’insuline dite » retard » qui peut être administrée avec une fréquence diminuée. Ces produits dominent aujourd’hui largement le marché.
En parallèle aux études sur les protéines, une collaboration fructueuse entre immunologistes et généticiens a permis de comprendre comment des anticorps étaient capables de reconnaître spécifiquement leur substrat. Ces travaux ont conduit à envisager l’utilisation d’anticorps contre des cibles moléculaires précises que l’on savait être impliquées dans certaines pathologies. L’idée est ici de bloquer la fonction d’une protéine cible.
De multiples difficultés, mais pas insurmontables
L’utilisation de protéines ou d’anticorps en tant que médicament se heurte à un certain nombre de difficultés.
Les approches antitumorales
Souvent les processus tumoraux sont liés à la surexpression de certains gènes. La spécificité des oligonucléotides peut être exploitée pour diminuer l’expression de ces gènes ou pour bloquer la fonction des protéines produites. D’autres approches visent à bloquer au niveau de la tumeur la formation de vaisseaux sanguins nécessaires pour son irrigation et sa croissance.
Tout d’abord, la production d’une protéine, qui peut se faire dans des bactéries, des levures, des cellules humaines, voire des animaux, peut poser des problèmes de stabilité ou de solubilité.
L’administration de la protéine, qui doit souvent se faire par voie intraveineuse, ne permet d’atteindre que le compartiment sanguin, les protéines ne diffusant pas librement à travers les membranes cellulaires.
Enfin, cette administration risque d’induire chez le patient une réaction immunitaire, notamment pour les anticorps.
De nombreux travaux d’ingénierie cellulaire et moléculaire ont été entrepris afin d’améliorer la sélectivité, la spécificité, la biodisponibilité et les propriétés pharmacocinétiques des anticorps, tout en diminuant leur pouvoir immunogène.
Ainsi les premiers anticorps, dits monoclonaux car ils dérivent d’une seule cellule, ont cédé la place à de nouvelles versions améliorées : par exemple, on » humanise » des anticorps de souris1, on se limite à l’utilisation de » fragments » possédant l’activité recherchée, on crée des protéines dites de » fusion » qui lient les propriétés de reconnaissance de l’anticorps avec d’autres protéines leur conférant une activité accrue, on conçoit des protéines totalement artificielles en partant du squelette d’une protéine connue.
Quand l’ADN devient médicament
Une autre approche consiste à tenter d’utiliser de courts fragments d’acides nucléiques, appelés oligonucléotides, comme médicaments2. Cette idée est née du constat établi au début des années quatre-vingt que de courts oligonucléotides, appelés » antisens « , peuvent en se fixant sur un ARN messager conduire à sa dégradation.
L’approche » antisens » est aujourd’hui supplantée par une approche plus efficace appelée interférence à ARN (RNAi). L’introduction de courts ARN en double brin dans des cellules aboutit, par un mécanisme enzymatique en plusieurs étapes, à la dégradation des ARN messagers contenant la séquence de l’un des deux brins complémentaires.
Utiliser comme médicament de courts fragments d’ADN
Dans les deux cas, l’expression du gène ciblé est inhibée de manière spécifique, car l’ARN détruit ne pourra plus conduire à la production d’une protéine fonctionnelle. Les aptamères sont des oligonucléotides qui se fixent non pas sur des ARN, mais sur des protéines.
Leur séquence est choisie à l’issue d’un processus de sélection complexe impliquant une grande quantité de séquences différentes, ce qui permet d’isoler les séquences en fonction de leur aptitude à se fixer sur la cible choisie. La fixation de l’aptamère sur la protéine aboutit à inhiber la fonction de la protéine.
Avastin, un très grand succès
D’après une étude de Datamonitor3, les ventes de produits biothérapeutiques représentaient 26 milliards de dollars en 2007 et devraient croître jusqu’à 49 milliards de dollars en 2013.
Les analystes financiers prédisent que, d’ici 2015, Avastin, l’anticorps monoclonal anticancéreux de Genentech et Roche, sera le médicament qui générera le plus grand revenu de l’histoire de l’industrie.
Comme les protéines, les oligonucléotides traversent mal les membranes cellulaires, un problème crucial puisque leurs cibles sont situées dans les cellules. De plus, ces molécules sont rapidement dégradées et éliminées. Il est possible d’améliorer la stabilité et la biodisponibilité des oligonucléotides grâce à l’introduction de modifications chimiques. Une des difficultés est d’introduire ces modifications tout en préservant l’activité biologique. Plusieurs oligonucléotides ont fait l’objet d’un développement assez poussé sur des modèles de cellules en culture ou des modèles animaux. L’inhibition spécifique de l’expression d’un gène a pu être observée en administrant des ARN interférents à des souris par voie intraveineuse.
Une importance commerciale
Les produits biothérapeutiques sont convoités assidûment par l’industrie pharmaceutique. Commercialement, ces produits constituent une part importante des revenus de l’industrie, et bénéficient d’une forte croissance, de larges marges de profit et d’une faible compétition générique.
Jusqu’à présent, les avancées scientifiques dans le domaine biothérapeutique ont été exploitées par de jeunes entreprises » biotech » qui se sont approprié la propriété industrielle et ont développé les premiers produits. Si certaines entreprises pharmaceutiques ont développé en interne des produits biothérapeutiques, tel Eli Lilly avec l’insuline, beaucoup de sociétés ont choisi d’acquérir leurs compétences et produits de façon externe, sous la forme de partenariat ou d’acquisition.
Des prises de position stratégiques
Beaucoup de sociétés ont choisi d’acquérir leurs compétences et produits de façon externe, sous la forme de partenariat ou d’acquisition
Étant donné le potentiel commercial d’une nouvelle génération de biothérapeutiques, les grands groupes pharmaceutiques se livrent à une compétition intense, et prennent des positions stratégiques dans l’espoir de dominer une approche particulière.
La plupart d’entre eux essaient de combiner des acquisitions qui permettent de contrôler une technologie avec quelques partenariats qui permettent de ne pas être exclus d’autres domaines.
La relation entre Roche et Genentech, établie en 1990, reste un modèle de l’avantage qu’il y a à investir tôt dans des biothérapeutiques. Roche a choisi de contrôler une partie du capital de Genentech mais de laisser l’entreprise indépendante. En contrepartie, Roche a eu le droit de commercialiser en Europe les produits découverts par Genentech. En 2007, les produits issus de Genentech constituaient 58 % du revenu généré par les vingt meilleurs produits de Roche5 et les trois meilleurs produits vendus par Roche venaient de Genentech. Récemment Roche a annoncé l’intention d’acquérir le reste du capital de Genentech et de fusionner les deux compagnies. Roche ne s’est pas contenté de ce succès dans le domaine des protéines thérapeutiques et des anticorps monoclonaux.
La compagnie a aussi misé fortement sur l’interférence à ARN avec l’acquisition des biens et brevets européens de Alnylam qui lui ont permis de fonder un centre de recherche dans le domaine. Roche a aussi pris position dans le domaine des aptamères à travers un partenariat avec la biotech allemande Noxxon.
Quelques exemples
Bristol-Myers Squibb (BMS) a choisi en 2006 d’acquérir Adnexus, qui développe les » adnectins » (protéines formées sur un squelette de fibronectine) pour se donner une capacité interne de découverte de protéines thérapeutiques. Bristol-Myers Squibb avait auparavant établi une collaboration avec Domantis pour la découverte de fragments d’anticorps, mais s’était vu par la suite exclu de la technologie par l’acquisition de Domantis par GlaxoSmithKline (GSK). BMS a récemment tenté d’acquérir ImClone pour étendre ses capacités dans le domaine des anticorps monoclonaux, mais s’est vu surenchéri par Eli Lilly. Afin de ne pas être exclu des ARN » antisens « , BMS a établi une collaboration avec Isis Pharmaceuticals, un des leaders dans le domaine avec près de vingt ans d’expérience.
Merck constitue un autre exemple intéressant. La compagnie a fait grand bruit en achetant pour 1,1 milliard de dollars en 2006 Sirna, un des leaders dans la technologie des RNAi. Pour Merck, qui était traditionnellement orienté vers les petites molécules, Sirna constituait une entrée dans le monde des biothérapeutique4, et d’autres prises de position sont à prévoir.
De grands espoirs pour l’avenir
De grands espoirs ont été introduits par les biothérapeutiques dans des maladies assez répandues, en particulier la dégénérescence maculaire
Malgré les nombreux problèmes que leur utilisation soulève, les protéines et les anticorps ont permis, en l’espace de deux décennies, de considérables progrès dans le domaine de la recherche fondamentale et, plus récemment, ont conduit à des bénéfices thérapeutiques importants, notamment dans le traitement de cancers et de maladies inflammatoires.
Contrairement aux anticorps, peu d’oligonucléotides ont été mis sur le marché, mais les nombreux essais cliniques en cours témoignent de l’effervescence de ce domaine et permettront de valider les efforts entrepris.
De grands espoirs ont été introduits par les biothérapeutiques dans des maladies assez répandues et pour lesquelles les approches étaient jusqu’ici très limitées. C’est le cas de la dégénérescence maculaire liée à l’âge, pour laquelle ont été mis sur le marché récemment un anticorps et un aptamère.
Les progrès de la biologie moléculaire laissent à penser que la découverte de nouvelles générations de biothérapeutiques n’est pas prête de ralentir. Les exemples d’approches nouvelles à fort potentiel ne manquent pas comme les miRNA, les méganucléases (voir l’article de D. Sourdive dans ce numéro), les Zinc Fingers et les Unibodies.
En même temps, l’industrie pharmaceutique semble loin d’être rassasiée, et reste à l’affût des technologies capables de générer les médicaments de demain.
1. D. BELLET & V. DANGLES-MARIE (2005), Anticorps humanisés en thérapeutique, Médecine-Sciences, vol. 21, p. 1054–1062.
2. Y. FICHOU & C. FÉREC (2006), The potential of oligonucleotides for therapeutic applications, Trends in Biotechnology, vol. 24, p. 563–569.
3. Datamonitor report : Monoclonal Antibodies Report : 2008 Update – Detailed analysis of the monoclonal antibody segment, encompassing market dynamics, key therapy areas, technology and target types through to 2013, evaluating the strategies companies are using to capitalize on this lucrative market.
http://www.datamonitor.com/Products/Free/Report/DMHC2427/020DMHC2427.htm
4. « Merck Buys Maker of Gene-Silencing Drugs », New York Times, October 31, 2006.
http://query.nytimes.com/gst/fullpage.html?res=9C00E1DB123FF932A05753C1A9609C8B63
5. Article : « Roche’s Opportunity », BioCentury, July 28, 2008. Volume 16, number 34.