L’effet des faibles doses

Pour des doses de l’ordre de 500 mSv1 en irradiation aiguë ou chronique on a constaté, chez l’animal comme chez l’homme, une augmentation de la fréquence des leucémies et de quelques autres cancers et un risque de malformation quand l’embryon a été irradié pendant la gestation, etc. Aucun effet nuisible n’a été détecté chez l’adulte pour des doses inférieures à 200 mSv et chez l’enfant pour des doses inférieures à 100 mSv, ni aucune malformation pour des doses inférieures à 200 mSv.
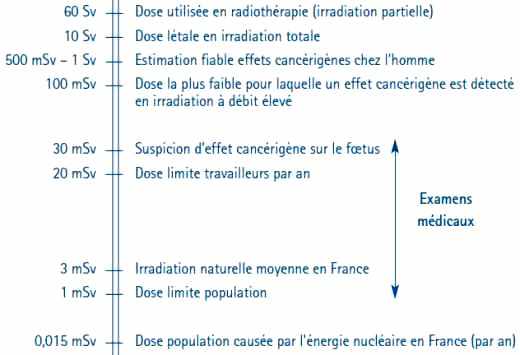
On appelle faibles doses, les doses inférieures à 100 mSv, et très faibles doses, celles de quelques mSv ou moins, c’est-à-dire de l’ordre de grandeur de l’irradiation naturelle à laquelle est soumis tout être vivant depuis l’origine de la vie sur Terre, soit quatre milliards d’années, période pendant laquelle la radioactivité naturelle a diminué d’environ un facteur 4.
En France, l’irradiation naturelle annuelle varie selon les régions de 1,5 à 6 mSv et, dans le monde, elle varie de 1,5 mSv à 30 mSv, voire même dans certaines régions d’Iran 200 mSv/an. En regard, les doses délivrées au cours des examens médicaux vont de 0,1 mSv à 20 mSv ; les doses dues à la production de l’énergie nucléaire sont pour les travailleurs en moyenne d’environ 2 mSv/an (moins de 1 % d’entre eux reçoivent, en un an, une dose égale ou supérieure à 20 mSv) et pour le public plus de cent fois plus petites, environ 0,015 mSv/an (en y incluant l’extraction et le traitement de l’uranium, le fonctionnement des réacteurs, les rejets et les déchets).
C’est la valeur qui a été estimée dans le Cotentin au voisinage immédiat de La Hague, et elle n’est qu’exceptionnellement et faiblement dépassée dans quelques autres zones très limitées de la France. La directive de 1996 de l’Union européenne fixe une limite annuelle de dose égale pour les travailleurs à 100 mSv/5 ans, soit en moyenne 20 mSv/an et de 1 mSv/an pour le public (tableau 1).
La vie d’une cellule, ses réactions après une modification du milieu sont régies par des instructions codées dans les molécules d’ADN (acide désoxyribonucléique) qui forment le génome de chaque cellule. Ce génome renferme environ 50 000 gènes et est identique dans toutes les cellules d’un organisme humain ; mais à chaque instant dans une cellule, seul un petit nombre de gènes sont en activité, les autres pouvant l’être quand ils en reçoivent l’ordre.
Dans un tissu adulte, quand une cellule meurt, l’ordre est donné à une autre cellule de se diviser de façon à maintenir constant le nombre de cellules. Ce mécanisme de régulation est perturbé dans les cellules cancéreuses qui se divisent sans en avoir reçu l’ordre.
La transformation d’une cellule normale en cellule néoplasique est due au dysfonctionnement d’une dizaine de gènes parmi les quelques centaines qui interviennent dans la régulation de la division cellulaire. Une tumeur cancéreuse est constituée par les descendants de cette cellule transformée (c’est pourquoi on dit d’un cancer qu’il est monoclonal). Les molécules d’ADN sont constituées par deux fibres, ou brins, enroulés l’un autour de l’autre et qui sont complémentaires. L’ordre des bases sur ces brins constitue le code qui détermine la constitution de la protéine dont la synthèse est régie par ce gène. Le remplacement d’une base pour une autre change donc cette constitution et peut altérer la fonction de cette protéine et donc celle de la cellule.
Le dysfonctionnement d’un gène est généralement dû à une mutation, c’est-à-dire à une modification irréversible et transmissible aux cellules filles, de la molécule d’ADN qui porte ce gène. Les molécules d’ADN sont longues (4 cm) et étroites (2 nm), elles sont donc très fragiles ; les lésions de l’ADN sont fréquentes et une proportion considérable du génome (le quart environ) est consacrée à la détection et la réparation des lésions, c’est-à-dire au maintien de l’intégrité du génome.
Les rayonnements ionisants ne délivrent que des énergies très faibles aux cellules irradiées, mais cette énergie est concentrée le long des trajectoires des particules et peut donc léser les molécules d’ADN soit en ionisant l’un des atomes de cette molécule (dans un tiers des cas) soit dans deux tiers des cas en provoquant la formation au voisinage de la molécule d’ADN de radicaux libres, agents d’oxydation puissants.
Le métabolisme normal d’une cellule provoque également la formation de radicaux libres. Ceux-ci causent, chaque jour, dans chaque cellule, environ 17 000 lésions dont 10 000 cassures de l’un des deux brins d’une molécule d’ADN et 8 cassures des deux brins. En comparaison, une dose de 1 gray provoque, dans chaque cellule, 1 000 ruptures de l’un des brins et 40 ruptures des deux brins mais concentrées dans l’espace et le temps. Les cassures d’un seul brin sont facilement réparées car la cellule prend comme modèle le brin intact. La réparation des cassures des deux brins est beaucoup plus difficile puisque les deux brins sont lésés.
Les effets cancérigènes des faibles doses : la relation linéaire sans seuil
L’absence d’effet détectable, après les faibles doses, ne permet pas d’exclure l’existence d’un risque cancérigène trop petit pour être mis en évidence par les études statistiques. Par prudence, et tout en soulignant qu’il ne s’agissait que d’une hypothèse commode, la Commission internationale de protection contre les radiations (CIPR) avait proposé, au début des années 1960, d’estimer ces risques par une extrapolation linéaire à partir des effets observés entre 0,5 et 3 Sv.
La relation linéaire a, en outre, l’avantage de simplifier l’enregistrement des données puisqu’elle permet l’addition au cours de la vie des diverses irradiations professionnelles. Elle fut donc bien accueillie par ceux qui gèrent la radioprotection, d’autant qu’elle surestime les risques, ce qui constitue un autre avantage de ce point de vue.
Quinze ans plus tard, la découverte des oncogènes et de la transformation d’un gène normal (proto-oncogène) en oncogène par une simple mutation parut donner un fondement scientifique à cette hypothèse qui devint alors un dogme, surtout dans certains milieux de la radioprotection n’ayant que peu de formation en biologie.
En réalité une extrapolation d’un facteur 10 est acceptable scientifiquement en biologie, mais elle est très discutable sur un facteur 100 et n’a aucun sens sur un facteur 1 000 ou 10 000 car dans un organisme vivant toute action suscite une réaction, ce qui change les conditions. Dès le milieu des années 1980, des radiobiologistes s’interrogèrent donc sur la validité scientifique de cette extrapolation.
Son utilisation pour calculer le risque de faibles doses suscita des réticences qui s’accentuèrent quand, après l’accident de Tchernobyl, on calcula avec une précision absurde, le nombre de cancers que les retombées radioactives causeraient en Europe. L’Académie des sciences puis l’American Health Physics Association dénoncèrent, dans des rapports, cette utilisation abusive. Tout le débat sur les effets éventuels des faibles doses se focalisa ainsi sur cette question. Il nous faut donc expliciter et discuter les trois hypothèses sur lesquelles elle est fondée :
1) Toute lésion du génome a une probabilité égale de provoquer une altération irréversible et transmissible du génome (une mutation), donc d’initier une transformation néoplasique de la cellule, qu’elle soit isolée ou associée à d’autres lésions dans la même cellule et les cellules voisines.
2) Certaines lésions complexes de l’ADN provoquées par des rayonnements ionisants ne sont pas réparables sans erreur. Toute traversée du noyau d’une cellule par une particule ionisante a donc une probabilité non nulle de provoquer une mutation.
3) Le cancer est dû à la sommation de plusieurs mutations. Celles causées par les radiations s’associent à celles d’autres origines et il existe une proportionnalité directe entre le nombre de mutations et la fréquence des cancers.
Examinons ces trois hypothèses.
Influence sur l’évolution d’une lésion de l’ADN de la présence d’autres lésions dans la même cellule ou les cellules voisines
Schématiquement une lésion de l’ADN peut :
- entraîner la mort de la cellule ou l’incapacité de division,
- être réparée sans erreur,
- être réparée avec erreur ou ne pas être réparée, il en résulte donc une mutation.
Dans les deux premiers cas, le risque cancérigène est nul puisque la lésion n’existe plus. La mort d’une cellule n’a pas de conséquence si le nombre de cellules tuées est petit puisque les mécanismes d’homéostasie tissulaire provoquent la division d’autres cellules afin de remplacer la cellule manquante. Dans le troisième, il existe une lésion transmissible aux cellules filles. L’hypothèse de la relation linéaire sans seuil implique nécessairement que l’efficacité d’une irradiation (nombre de lésions par unité de dose), et le risque de mutation, ne varient pas avec la dose et le débit de dose (dose par unité de temps). Ce n’est manifestement pas le cas et la CIPR a été obligée d’introduire un coefficient de réduction aux faibles doses et débits de dose égal à 2, valeur discutable (les données expérimentales montrent des réductions allant de 2 à 10).
Il est, aujourd’hui, certain qu’après une irradiation la mort des cellules et les mutations sont dues aux lésions des deux brins.
Trois mécanismes de réparation de ces lésions ont été identifiés. Dans le premier, la cellule va chercher un modèle sur l’autre molécule d’ADN homologue (dans une cellule normale chaque molécule d’ADN est en deux exemplaires dont l’un provient du père et l’autre de la mère). Des erreurs peuvent survenir mais sont relativement rares. Les deux autres mécanismes de réparation sont beaucoup plus sujets à erreur. Il paraît vraisemblable (il y a beaucoup d’arguments dans ce sens, mais ceci n’est pas formellement démontré) que le mécanisme de réparation le plus fiable est le premier mis en œuvre, les moins sûrs étant activés quand les lésions sont plus nombreuses. Ceci s’accorderait avec l’observation selon laquelle la fréquence des réparations fautives croît avec la dose.
De plus on a montré au cours de ces dernières années que des doses relativement faibles (de 10 à 200 mGy) suffisent à provoquer des modifications de la signalisation intra et intercellulaire. Donnons-en quelques exemples :
- stimulation de la détoxification des radicaux formés sous l’action des rayonnements ionisants ;
- arrêt temporaire de la progression des cellules dans le cycle cellulaire, ce qui favorise la réparation de l’ADN car celle-ci est plus efficace dans les cellules au repos ;
- activation de nombreux gènes impliqués dans les mécanismes de réparation de l’ADN. On observe de tels effets pour des doses aussi petites que 10 mGy (rappelons qu’une cassure des deux brins requiert une énergie de 25 mSv, donc pour une dose moyenne de 10 mSv la proportion de cellules avec une cassure double est petite).
Il est donc vraisemblable que les premières doses de rayonnement modifient la proportion de cassures des deux brins réparées par les trois mécanismes existants, donc la proportion de lésions évoluant soit vers une réparation non fautive soit vers une mutation. De plus, on a constaté une diminution de l’efficacité des systèmes de réparation quand le nombre de lésions est trop élevé.
Relation entre la dose et la mortalité cellulaire
La variation de la capacité de réparation des lésions en fonction de la dose a été mise en évidence par l’étude du taux de mortalité.
Lors d’une irradiation continue à débit de dose élevé (1 Gy/min), on distingue trois domaines de radiosensibilité :
- entre 0 et 0,3 Gy, il existe une hypersensibilité : le taux de mortalité par unité de dose est relativement très élevé mais il décroît avec la dose ;
- à partir de 0,3 Gy, la radiosensibilité est beaucoup plus faible, mais elle augmente progressivement jusqu’à 5 Gy (ce qui correspond à l’épaulement de la courbe) ;
- au-delà de 5 Gy, la radiosensibilité est constante, la courbe devient exponentielle.
On a interprété ainsi ces résultats :
- pour les doses inférieures à 0,3 Gy, la plupart des cellules dont l’ADN a été lésé meurent ; cependant quand la dose augmente la capacité de réparation des lésions s’accroît à cause de l’activation de mécanismes de réparation ;
- entre 0,3 et 5 Gy, la capacité de réparation est d’abord maximale, puis elle diminue progressivement, comme s’il y avait épuisement, ou saturation, de la capacité de réparation ;
- après environ 5 Gy, cette capacité est faible et ne varie plus. L’adminis-tration d’inhibiteurs de la synthèse des protéines (donc des enzymes) réduit ces variations et augmente la radiosensibilité.
Si l’irradiation est interrompue, la capacité de réparation augmente rapidement et redevient maximale après une interruption d’environ huit heures. Ces résultats montrent l’importance des variations de capacité de réparation des lésions doubles brins en fonction de l’activation ou de la saturation des systèmes enzymatiques.
Dans les lignées cellulaires qui sont incapables de réparer les lésions des deux brins du fait d’un défaut génétique, la courbe est d’emblée exponentielle : la radiosensibilité est constante et est grande.
Lors d’irradiation à faible débit (quelques mGy/minute ou moins) la courbe est exponentielle, ce qui signifie que la capacité de réparation est constante. Si les cellules, au lieu d’être irradiées isolées les unes des autres, sont irradiées en amas (sphéroïdes) donc liées entre elles, comme dans un tissu, par des canaux de jonction qui permettent la circulation des petites molécules d’une cellule à l’autre, la radiosensibilité est notablement diminuée. Les cellules avoisinantes participent donc au système de réparation.
Les cellules engagées dans un cycle de division cellulaire réparent moins bien les lésions de l’ADN que les cellules au repos mitotique. Un des premiers effets de l’irradiation d’une cellule saine est d’interrompre sa progression dans le cycle cellulaire de façon à donner à la cellule le temps de réparer ses lésions avant la division cellulaire, moment où elles sont transmises aux cellules filles.
Les mécanismes d’adaptation démontrent également la capacité de réaction après une irradiation. On a constaté, depuis une vingtaine d’années, qu’une première irradiation à faible dose (quelques dizaines de mGy) réduit considérablement la mortalité des cellules, ou de l’organisme, lors d’une irradiation à dose beaucoup plus forte (quelques Gy) délivrée quelques heures, ou jours plus tard. Cette protection semble s’expliquer par la stimulation temporaire de mécanismes de réparation. Elle semble protéger également contre l’induction de mutations pouvant évoluer vers une transformation cancéreuse.
Mécanismes de sauvegarde du génome et relation entre la dose et la probabilité de mutation
À côté de la réparation des molécules d’ADN, la mort cellulaire constitue un autre système de protection de l’organisme. À faible dose, l’hypersensibilité cellulaire a pour résultat l’élimination de la plupart des cellules lésées. À doses plus élevées, l’apoptose, ou mort programmée, joue le même rôle. Il semble que l’efficacité de ces systèmes diminue avec la dose.
Il existe plusieurs mécanismes de mort cellulaire :
- par anoxie ou effet toxique ;
- par sénescence au terme de l’existence normale de ce type de cellules (par exemple un jour pour le granulocyte, quatre mois pour les globules rouges) ;
- enfin, la mort programmée ou apoptose. Celle-ci joue un rôle important au cours de l’embryogenèse : par exemple les doigts se forment à la suite de la mort des cellules situées dans les espaces interdigitaux. L’apoptose élimine les cellules dont l’ADN n’a pas été réparé de façon satisfaisante. Elle joue un rôle capital dans la protection de l’organisme contre les agents génotoxiques. En effet, laisser subsister une cellule dont l’ADN a été lésé mais qui est néanmoins capable de se diviser peut être à l’origine de plusieurs maladies mortelles (cancers, maladies auto-immunes, etc.).
Pour beaucoup d’auteurs, pour des doses de l’ordre de grandeur de l’irradiation naturelle, c’est-à-dire quand les deux mécanismes de réparation et d’apoptose ne sont pas saturés ou désorganisés par de nombreuses lésions, l’association du système de réparation de l’ADN et de l’apoptose suffit à éliminer la quasi-totalité des lésions pouvant être à l’origine d’une mutation. Signalons que, par ailleurs, l’altération de l’apoptose qui permet, au fil des générations cellulaires, l’accumulation de mutations dans le génome d’une lignée cellulaire joue un rôle capital en cancérogenèse.
La relation entre la dose et la probabilité de mutation est moins bien connue que celle concernant la mortalité, techniquement plus facile à étudier dans le domaine des faibles doses. Néanmoins, quelques faits ont été établis :
- relation entre la dose et l’altération de la morphologie des chromosomes (nombre de chromosomes dicentriques) : pas d’anomalie pour des doses < 20 mGy, relation linéaire entre 0,5 Gy et 5 Gy ;
- en ce qui concerne la formation de cellules avec micronoyaux, pas d’augmentation de leur fréquence au-dessous de 0,2 Gy et relation linéaire entre 0,2 et 2 Gy ;
- pour les transformations néoplasiques in vitro, on n’observe rien pour des doses inférieures à 100 mGy et pour les mutations somatiques rien au-dessous de 200 mGy. (Rappelons qu’une dose de 1 mGy correspond, en moyenne, à la traversée du noyau cellulaire par un électron avec pour conséquence une lésion simple brin.)
Ainsi, tant ce qui concerne la mortalité cellulaire que les mutations, les faits diffèrent des prédictions de la relation linéaire sans seuil :
- l’influence de la dose et du débit de dose est très grande, elle a pour résultat des changements importants de radiosensibilité (mortalité) qui sont la conséquence des variations de capacité de réparation des lésions de l’ADN, notamment des lésions doubles brins ;
- le stress génotoxique déclenche la stimulation de mécanismes de réparation après des doses supérieures à une dizaine de mGy et l’existence de phénomènes d’adaptation confirme que de faibles doses peuvent activer des mécanismes de réparation qui sont normalement au repos ;
- pour certains effets, tels que la probabilité de mutation, il semble exister un seuil pratique dû à la conjonction d’une réparation sans erreur et d’une apoptose éliminant les lésions résiduelles ;
- l’augmentation de la dose et surtout du débit de dose entraîne un débordement des capacités de ces systèmes d’où l’augmentation considérable de la radiosensibilité (jugée sur le taux de mortalité), des réparations fautives et des aberrations chromosomiques (existence d’un seuil pratique ?).
Bien qu’il reste beaucoup de progrès à faire, il apparaît déjà certain que le premier postulat sur lequel est fondée la relation linéaire sans seuil est contredit par les données expérimentales.
Existe-t-il des lésions de l’ADN si graves qu’elles sont irréparables sans erreur et donnent naissance à des lignées mutantes ?
Les particules α et les neutrons sont les particules qui, par unité de longueur de trajectoire, transfèrent au milieu le plus d’énergie, créent le plus de dommage, celles qui au cours de la traversée des molécules d’ADN déterminent les lésions les plus complexes, c’est pourquoi leur efficacité biologique relative est si élevée.
Or les radioéléments naturels (radium, thorium) sont des émetteurs a, qui ont été utilisés depuis le début du XXe siècle. On dispose donc d’un long recul pour évaluer leur effet cancérigène. Quelques cohortes sont particulièrement intéressantes.
a) Les peintres en cadran lumineux : les quelques milliers d’ouvriers et ouvrières contaminés ont été minutieusement suivis. On a observé, chez eux, une cinquantaine d’ostéosarcomes des os de la face et la relation dose-effet montre l’existence d’un seuil pratique : aucun cancer n’a été observé pour des doses inférieures à 5 Gy alors que la fréquence de ces cancers augmente rapidement ensuite ; cette irradiation est donc, à dose élevée, très carcinogène. Cette courbe est compatible avec une relation quadratique, mais incompatible avec une relation linéaire. Les données expérimentales (Raabe) montrent que, selon l’espèce animale et le radioélément utilisé, le seuil pratique d’induction des tumeurs varie, mais il est toujours supérieur à 1 Gy. Rappelons que la dose absorbée lors de la traversée d’une cellule par un α est d’environ 370 mSv. Quand la dose et le débit de dose sont faibles, les cellules irradiées sont donc environnées de cellules intactes.
b) Les sujets ayant reçu du thorotrast (un composé à base de thorium) comme agent de contraste en radiologie vasculaire : des enquêtes effectuées en Allemagne, au Danemark et au Portugal ont révélé chez eux un pourcentage élevé de cancers du foie mais aucun effet n’a été décelé pour des doses inférieures à quelques Gy (plusieurs dizaines de Sv si l’on tient compte du facteur qualité égal à 20).
c) Les mineurs des mines d’uranium respirent un air riche en radon et, depuis le XVIIIe siècle, on a constaté chez eux une forte augmentation de la fréquence des cancers du poumon. On a longtemps cru qu’il existait, dans ce cas, une relation linéaire sans seuil entre les quantités de radon inhalées et la fréquence de ces cancers. Cette conclusion est remise en question car il existe dans l’air des mines d’autres agents cancérigènes (en particulier l’arsenic2, et des poussières radioactives. De plus ces sujets reçoivent une irradiation importante due au rayonnement gamma. Ces facteurs pourraient expliquer pourquoi la fréquence des cancers, à quantité égale de radon inhalé, varie considérablement d’une mine à l’autre et pourquoi on n’a pas détecté une augmentation de la fréquence des cancers du poumon chez les habitants des régions où l’air est riche en radon.
Les expériences ont, par ailleurs, montré l’influence importante du débit de dose sur l’effet cancérigène. À quantité égale de radon inhalé (25 WLM3, les rats présentent des cancers pulmonaires si la dose est administrée en cinq mois alors qu’aucun effet n’est détecté si elle est administrée en dix-huit mois. Les calculs effectués suggèrent que les cellules dont le noyau a été traversé par une seule particule α ne se cancérisent pas et que la cumulativité des effets dépend de l’intervalle de temps entre les traversées. Il y a deux explications possibles à cette absence d’effet cancérigène pour les faibles doses et débits de dose :
- les lésions provoquées par les faibles doses sont réparées ou la cellule éliminée. Une récente expérience effectuée avec des microfaisceaux de particules a sur des cellules en culture confirme l’absence de transformation néoplasique après la traversée par une seule particule, alors qu’il en existe après plusieurs particules comme si, alors, la capacité des mécanismes de protection avait été outrepassée ;
- l’évolution d’une cellule mutée vers un cancer est contrôlée si les cellules adjacentes sont intactes. Dans ce cas la division cellulaire peut être inhibée, or la multiplication cellulaire joue un rôle essentiel dans le processus cancérigène. La plus grande cancérogénicité des irradiations par neutrons est en faveur de cette hypothèse car dans ce cas, toutes les cellules du tissu sont lésées simultanément.
Les deux hypothèses ne s’excluent d’ailleurs pas. Ce que les irradiations par particules α ont démontré est que des lésions isolées dans une seule cellule d’un tissu n’ont qu’un faible risque d’évoluer vers un cancer, contrairement au postulat de la relation linéaire sans seuil. À très faibles doses de photons (quelques mGy), la cellule touchée est également entourée de cellules saines.
Processus cancérigène : relation entre le nombre des cellules initiées et celui des cancers
Quel que soit le nombre d’altérations du génome responsable de la transformation d’une cellule saine en une cellule néoplasique (certaines mutations pouvant être dues à l’irradiation et d’autres à des causes » naturelles »), la relation linéaire sans seuil postule une proportionnalité entre le nombre de cellules » initiées » et le nombre de cancers, autrement dit chaque cellule initiée, quelles qu’aient été les causes de cette initiation, a la même probabilité de donner naissance à un cancer.
Ce raisonnement paraît si logique qu’il a été long à être remis en question. On ne l’a fait que quand on a montré que la naissance d’un cancer ne pouvait pas être due à la sommation, par hasard, des 8 à 10 altérations distinctes des gènes dont l’atteinte est à l’origine du cancer. Si tel était le cas, en effet la probabilité de cancérisation serait tellement faible qu’il n’y aurait, dans le monde, qu’un ou deux cancers par génération. Inversement, la mutation de l’un des gènes responsables est un phénomène fréquent, qui touche un grand nombre de cellules.
Pour expliquer l’atteinte de plusieurs gènes spécifiques, il faut postuler un très grand nombre de divisions de la cellule initiée et un accroissement considérable de la probabilité de mutation de ces cellules lors de chaque division : donc une instabilité génétique associée à une amplification clonale. L’instabilité génétique peut être due à l’atteinte des mécanismes de maintien de l’intégrité du génome cellulaire (réparation de l’ADN, apoptose, etc.) ou à l’augmentation du taux d’agents d’oxydation.
Pour expliquer l’amplification clonale, prenons l’exemple des cancers de la peau sous l’influence des rayons ultraviolets du soleil. Une proportion élevée des cellules de la couche basale de l’épiderme présente des lésions dans leur génome, en particulier du gène p53 qui joue un rôle crucial dans l’apoptose. Le nombre de cellules initiées dont le mécanisme d’apoptose a été lésé est donc grand. Lors de chaque nouvelle exposition solaire, de nombreuses cellules subissent une nouvelle altération de leur génome.
Dans les lignées cellulaires normales, où l’apoptose fonctionne correctement, les cellules dont la lésion n’a pas été réparée sont éliminées. Dans celles où l’apoptose est déficiente, ces cellules survivent. Les cellules initiées dont l’apoptose fonctionne mal ont donc un avantage sélectif par rapport aux cellules normales puisque ce sont elles qui se multiplient pour remplacer les cellules tuées ; c’est le phénomène d’amplification clonale. De fait après chaque été, on voit apparaître sur la peau exposée des lésions (dyskératoses) prénéoplasiques dont la quasi-totalité disparaîtra spontanément pendant l’hiver.
En effet, entre en jeu, alors, un autre mécanisme de protection puissant : la sénescence. Les cellules de mammifères n’ont qu’une capacité de division limitée, elles ne peuvent se diviser qu’environ 60 fois, parce qu’à chaque division les extrémités des chromosomes (télomères) se raccourcissent et quand celles-ci ont disparu, les cellules ne peuvent plus se diviser et meurent. Ce mécanisme élimine automatiquement les cellules vieillies dans lesquelles un grand nombre de lésions ont pu s’accumuler. Ce mécanisme de sauvegarde disparaît quand existe un autre défaut » l’immortalisation « .
Dans celle-ci, en raison de la réactivation d’un gène qui ne fonctionne normalement que pendant l’embryogenèse, le télomère ne se raccourcit plus à chaque division, la cellule est devenue immortelle. Quand une cellule initiée dont l’apoptose ne fonctionne plus devient en outre immortelle, il a été ainsi créé une lignée de cellules dont la cancérisation devient possible car de nouvelles lésions peuvent s’y accumuler, par exemple la perte des gènes inhibiteurs de la prolifération cellulaire (tel le gène Rb) qui sont des gènes récessifs, c’est-à-dire dont il faut détruire (ou muter) les deux exemplaires présents dans la cellule pour entraîner une perte de la fonction. Ainsi peut survenir, chez quelques sujets et après des délais qui se chiffrent généralement en plusieurs décennies, l’apparition de cellules pleinement cancéreuses.
Ce rappel explique que le facteur limitatif de la cancérogenèse n’est pas l’événement initial mais l’ensemble des événements ultérieurs que l’on regroupe sous le terme de promotion, étape pendant laquelle les phénomènes principaux sont la prolifération cellulaire et l’altération des liaisons entre les cellules (désorganisation tissulaire), puisque normalement le devenir de chaque cellule est contrôlé par les signaux venus des cellules voisines. De fait, les principaux facteurs cancérigènes révélés par l’épidémiologie sont non des agents mutagènes mais des facteurs de promotion comme l’alcool, l’irritation, l’inflammation ou la suralimentation.
Prenons l’exemple du tabac qui est, avec le soleil, le facteur cancérigène le plus étudié puisqu’il est à l’origine de 30 % des cancers chez l’homme. La relation dose-effet est E = k D2 t4,5 où » E » est le taux de cancer en excès, » k » une constante, » D » le nombre de cigarettes fumées par jour et » t » la durée (en années) du tabagisme. On voit le poids essentiel de la durée du tabagisme (phase de promotion). La relation avec la dose n’est pas linéaire mais quadratique. Le rôle de la promotion est souligné par l’évolution de la fréquence des cancers après arrêt du tabagisme : celle-ci diminue rapidement et après vingt ans est revenue à une valeur à peine légèrement supérieure à la normale.
Ainsi si l’on a fumé 20 cigarettes par jour de 17 à 37 ans, l’inhalation, pendant toute cette période, de quantités massives de cancérigènes ne laisse (si l’on a eu la chance de ne pas avoir eu de cancer auparavant) que des séquelles minimes : la promotion apparaît vingt fois plus importante que l’initiation, contrairement au postulat de la relation linéaire sans seuil. Or l’irradiation chronique est un facteur de promotion. Le facteur limitatif est non le nombre de cellules initiées mais la promotion.
Ainsi, aucun des trois postulats impliqués par la relation linéaire sans seuil n’est en accord avec nos connaissances actuelles. On conçoit qu’on ait pu les proposer en 1960. Ils ne sont plus acceptables aujourd’hui. Il nous faut donc examiner les données expérimentales et épidémiologiques d’un œil critique à la lumière des connaissances actuelles.
Données expérimentales
Depuis un demi-siècle, un grand nombre d’expériences ont été effectuées pour mesurer l’effet cancérigène des divers types de radiations. Depuis qu’on a pris conscience du rôle critique de la relation dose-effet pour l’évaluation des risques des faibles doses, un effort a été effectué par deux groupes pour rassembler et analyser l’ensemble des données disponibles.
Tanooka vient de publier les résultats d’une analyse de plusieurs dizaines de publications. Il en ressort l’absence d’augmentation de la fréquence des cancers chez l’animal pour des doses inférieures à 100 mSv et à dose égale une influence très forte du débit de dose.
P. Duport, à Ottawa, a entrepris, depuis trois ans, une tache titanesque : une méta-analyse de l’ensemble des expériences animales ayant étudié la radiocarcinogénèse, soit plus d’une centaine de travaux au cours desquels 85 000 animaux ont été irradiés, et sur lesquels 60 000 cancers ont été observés, comparés à 15 000 témoins. Les résultats préliminaires confirment l’absence d’augmentation de la fréquence des cancers pour des doses inférieures à quelques centaines de mGy de rayon X ou gamma.
Bien que l’on ne dispose pas encore de l’ensemble des résultats, il semble déjà que ces résultats concordants ne sont pas compatibles avec la relation linéaire sans seuil. Ils militent en faveur de l’existence d’un seuil pratique dont le niveau se situerait aux environs de 100 à 500 mGy en fonction du débit de dose, de la nature des particules et du tissu irradié.
Données épidémiologiques
De nombreuses données ont été acquises au cours de ces dernières décennies. Le principal argument en faveur de l’existence d’une relation linéaire sans seuil provenait de l’analyse de la fréquence des cancers chez les survivants d’Hiroshima et Nagasaki ; celle-ci apparaissait compatible avec une relation linéaire entre 200 mSv et 3 Sv.
| Tableau 2 Effets cancérigènes des rayonnements ionisants |
|
| Mortalité (par an) en France entre | |
| • Irradiation naturelle : dose 2,5 mSv par an Réduction concevable (maison à haute teneur en radon) |
0 et 6 000 0 et 600 |
| • Irradiation médicale : dose moyenne 1 mSv par an Réduction concevable (meilleures techniques, meilleurs appareillages) | 5 et 2 500
3 et 800 |
| • Énergie nucléaire (irradiation professionnelle + publique + déchets) : dose au public 0,010 mSv par an Réduction concevable ? |
0 et 25 0 et 5 |
|
Les limites supérieures de risque sont calculées à partir des coefficients de risque de l’ICRP et de la relation linéaire sans seuil. Ce sont celles qui sont indiquées dans beaucoup d’articles et de manuels qui les présentent comme une certitude. Les limites inférieures du risque sont calculées en supposant que les doses inférieures à 10 mSv/an ne sont pas cancérigènes ; ainsi elles s’accordent mieux avec les connaissances actuelles, or elles ne sont jamais mentionnées.
Ce tableau montre aussi le gain important qui pourrait résulter d’une meilleure radioprotection des malades et la faible amélioration de la santé publique qui serait obtenue en réduisant l’irradiation due à l’énergie nucléaire puisque les risques, éventuels, sont déjà très faibles. |
|
Cependant, depuis cinq ans, on a montré que la fréquence des leucémies dans cette population ne suivait pas une relation linéaire mais plutôt curvilinéaire (quadratique) avec un seuil pratique à 200 mSv. En ce qui concerne les tumeurs solides, ce n’est que depuis 1998 que l’on a remis en question l’existence d’une relation linéaire. En effet, on s’est alors aperçu que la sous-estimation des doses dues aux neutrons, qui était connue depuis une décennie, pouvait avoir pour conséquence une surestimation de l’effet des faibles doses de photons. Il apparaît donc vraisemblable que pour les tumeurs solides aussi la courbe pourrait être curvilinéaire.
En ce qui concerne les dizaines d’autres études, la plupart d’entre elles ont, à faible dose, une précision si médiocre qu’elles ne permettent ni d’exclure ni d’affirmer l’existence d’un seuil. Quelques enquêtes, cependant, ont atteint une puissance statistique suffisante pour exclure une relation linéaire sans seuil, notamment, comme nous l’avons vu, chez les sujets exposés à des radioéléments naturels (radium, thorium). Mais il s’agissait d’émetteurs α et on pouvait discuter de la validité de ces résultats pour les photons.
Pour ceux-ci, les calculs statistiques montrent qu’il fallait constituer des cohortes de plusieurs centaines de milliers de sujets pour obtenir des données robustes. Le problème paraissait donc sans espoir, mais tout a changé récemment. D’abord, la création de cohortes aussi vastes est maintenant devenue possible. La première étude au Centre international de recherche sur le cancer portait sur 100 000 travailleurs du nucléaire. L’incidence des cancers y était inférieure à celle observée dans la population mais l’intervalle de confiance était si large qu’on ne pouvait pas exclure une relation linéaire sans seuil. On a élargi l’étude pour englober 500 000 sujets et les résultats seront prochainement disponibles.
D’autres études portant sur 100 000 malades irradiés montrent la faisabilité de telles enquêtes, or en France seule on irradie environ 100 000 malades par an. Ces données sont de plus en plus exploitées et certaines d’entre elles, par exemple la fréquence des leucémies après administration d’iode radioactif, permettent d’affirmer que les résultats obtenus ne sont pas compatibles avec la relation linéaire sans seuil.
| Tableau 3— Comparaison des risques pour la santé entre systèmes énergétiques |
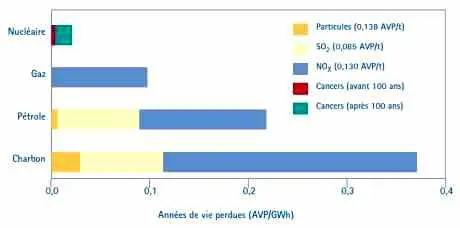 |
| Cette comparaison est basée sur les coûts-dommages par tonne de polluant évalués par le projet ExternE de la Commission européenne : graphique fourni par A. Rabl (France). Pour le nucléaire, le risque est calculé, à partir de la relation linéaire sans seuil, en tenant compte des effets cancérigènes et génétiques provoqués par l’irradiation subie par les travailleurs professionnels et par l’ensemble de la population (soit pendant cent ans, soit pendant trois mille ans). Ce type d’estimation surestime notablement les risques dus à l’irradiation à faible dose et donne une grande marge de sécurité. À l’opposé, ce type de calcul n’est pas utilisé pour les agents chimiques génotoxiques et cancérigènes produits par les autres agents. |
Mais le plus grand espoir pour évaluer l’effet des faibles doses réside dans la comparaison de l’incidence de certains cancers (en particulier les leucémies) dans les diverses régions du globe en fonction du niveau de l’irradiation naturelle. Celui-ci atteint ou dépasse 15 mSv/an voire 30 mSv/an dans certaines régions très peuplées, par exemple dans le sud de l’Inde, au Brésil et en Chine.
Ces études sont délicates à effectuer mais les premiers résultats, très encourageants, ne montrent aucune variation dans la fréquence des cancers en fonction de la dose d’irradiation naturelle. On peut déjà en conclure qu’il est illégitime d’utiliser la relation linéaire sans seuil pour évaluer les risques d’irradiation à dose de quelques mSv/an et a fortiori les doses d’une dizaine de microsieverts par an qui sont celles que reçoit la population française du fait du fonctionnement des centrales nucléaires.
Dans ces gammes de doses, l’utilisation de la relation linéaire sans seuil n’a aucune validité scientifique et l’estimation des risques fondée sur de tels calculs doit être proscrite. Il peut être utile pour rassurer la population de montrer que ces calculs pessimistes suggèrent des risques très faibles, mais il faut alors indiquer que les risques réels peuvent être très inférieurs et voire nuls (tableau 2). On ne l’a pas assez fait, par exemple à propos des risques de cancer de la thyroïde provoqués en France par les retombées de Tchernobyl.
Les calculs comparant les risques associés à la production d’énergie selon la filière utilisée indiquent que même avec ces calculs pénalisants les risques provenant de la filière nucléaire sont, en fonctionnement normal, très inférieurs à ceux calculés, sans recours aux hypothèses de la relation linéaire sans seuil, pour le charbon, le pétrole et le gaz (tableau 3). Pour le nucléaire, on inclut parfois les effets génétiques dans ces calculs, ceci ne serait admissible que si l’on introduisait ces mêmes risques génétiques pour les autres filières qui produisent également des génotoxiques aussi dangereux que les radioéléments, or ceci n’est pas fait. Rappelons que les enquêtes effectuées chez l’homme (notamment chez les descendants des survivants d’Hiroshima et Nagasaki soit environ 80 000 sujets ou sur ceux des malades irradiés à dose beaucoup plus élevée) n’ont décelé aucun effet génétique.
Il existe à propos des rayonnements ionisants des craintes latentes qui n’ont pas de fondement scientifique mais qui néanmoins entraînent une surestimation délibérée des risques pour accroître la marge de sécurité. Cette approche faite pour rassurer a paradoxalement augmenté l’inquiétude. Je prendrai deux exemples des conséquences néfastes de ces craintes irrationnelles. L’irradiation constitue une méthode très efficace pour stériliser certains aliments sans en changer leur goût ; ils n’ont bien entendu aucun effet nocif comme en attestent les documents de l’OMS ou de la Communauté européenne. Pour le poivre et les autres épices qui présentent des risques sanitaires (contamination bactérienne) importants quand ils ne sont pas stérilisés, l’irradiation était jusqu’à une date récente utilisée. Un règlement a rendu obligatoire la mention » stérilisée par ionisation « .
De peur d’un rejet du public, les fabricants y ont alors renoncé et utilisent des procédés moins efficaces. Autre exemple, l’eau de mer est relativement riche en uranium, à tel point qu’on envisage d’utiliser les océans comme une source quasi inépuisable pour la production d’énergie nucléaire. Or on envisage d’interdire tout rejet radioactif en mer alors que ceux-ci n’augmenteraient que de façon insignifiante la radioactivité des océans qui est de plus de 1022 Bq.
Conclusion
Les rayonnements ionisants à doses supérieures à quelques centaines de millisieverts provoquent une augmentation de la fréquence des cancers et à doses supérieures à quelques sieverts des lésions tissulaires qui peuvent être très invalidantes, voire mortelles. Mais aucun effet nocif n’a été décelé chez l’animal ou l’homme pour des doses inférieures à une centaine de mSv en irradiation aiguë et à 500 mSv en irradiation à faible débit ou encore à une dizaine de millisieverts par an en irradiation chronique pendant toute la durée de la vie.
Cette absence d’effet semble due au nombre et à la puissance des mécanismes de réparation et de sauvegarde du génome. La vie s’est développée dans un bain de rayons ionisants et d’ultraviolets ; très tôt sont apparus au cours de l’évolution (déjà sur les bactéries et les algues) des systèmes capables de maintenir l’intégrité du génome lors d’une irradiation à faible débit de dose, systèmes qui sont débordés quand le débit de dose est élevé (intervalle de temps court entre les agressions).
Aucun effet génétique n’a jamais été observé chez l’homme (ni chez les 80 000 descendants des survivants d’Hiroshima et Nagasaki ni chez les descendants des sujets irradiés pour des raisons médicales). Faute de données, on a calculé les risques génétiques chez l’homme à partir de ceux observés chez la souris sans tenir compte des mécanismes de protection plus puissants qui existent chez l’homme (élimination précoce des embryons anormaux). Par prudence, on surestime délibérément les risques de cancer et les effets génétiques.
Les règles de radioprotection actuelles ont été calculées pour offrir des marges de sécurité importantes et rendent très sûre l’utilisation industrielle ou médicale des rayonnements ionisants (à condition, bien entendu, qu’elles soient respectées). La Commission internationale de protection contre les rayonnements envisage actuellement de les modifier pour tenir compte de l’avancée des connaissances.
Le concept de dose collective va être, probablement, revu car l’idée que toutes les irradiations, même les plus faibles, peuvent être additionnées pour calculer un risque global n’est plus admissible puisqu’il est de plus en plus évident que les doses de l’ordre de grandeur de l’irradiation naturelle (quelques mSv/an) ne présentent aucun risque. De même, la notion de dose limite individuelle fixée à 1 mSv/an, soit à un niveau nettement inférieur à la variation de dose d’irradiation naturelle d’une région à l’autre de la France, sera sans doute, à terme, abandonnée au profit d’un autre concept : contrôler les émissions de radiations à la source.
Il est difficile de prévoir plus avant ce que seront les nouvelles règles mais tous les spécialistes estiment que le progrès des connaissances radiobiologiques et la non-validité de la relation linéaire sans seuil pour des doses inférieures à l’irradiation naturelle imposent un changement profond de doctrine. Il ne faut pas que les contraintes légitimes imposées par la radioprotection provoquent la peur de toute irradiation, car ceci pourrait avoir des conséquences fâcheuses pour la pratique médicale (crainte des examens radiologiques) comme pour la production d’énergie. Pour la radioactivité comme pour tous les agents chimiques ou physiques (rayons UV du soleil) » c’est, comme le disait Claude Bernard, la dose qui fait le poison « .
_________________________________________
1. La dose d’irradiation se mesure en gray (Gy). Un matériau reçoit une dose de 1 Gy quand l’énergie transférée par les rayonnements à la matière est de 1 joule par kg ; ce qui correspond approximativement à 2.1017 ionisations par kg, donc 2.105 ionisations dans une cellule (masse 10-9 g).
Pour tenir compte des variations d’efficacité biologique en fonction de la nature des rayonnements, on a introduit une autre unité le sievert (Sv) qui exprime la quantité de dommage biologique ou dose équivalente. La dose en Sv est égale à la dose en Gy multipliée par un facteur de qualité qui tient compte de l’efficacité biologique relative. Pour les rayons a par exemple Q = 20. Pour les rayons X ou g : Q = 1 dans ce cas la dose en Gy est égale à la dose en Sv.
On utilise aussi le sievert pour une autre grandeur, la dose efficace qui qui prend en compte la quantité et la nature des tissus irradiés (ce n’est pas la même chose de donner 1 Gy à un orteil ou à l’ensemble de l’organisme).
2. voir rapport UNSCEAR 1994
3. WLM : Working level month, c’est une unité pratique utilisée dans les mines.