Le cycle océanique du carbone : la machine thermodynamique et la jungle biologique

Le carbone, qui sous sa forme oxydée CO2 (ou encore dioxyde de carbone) est un gaz à effet de serre, est environ 50 fois plus abondant dans l’océan que dans l’atmosphère. Le dioxyde de carbone est une molécule très stable qui,dans l’atmosphère, ne réagit avec aucune autre.
De l’usage de l’énergie solaire (actuelle et fossile)
Dans les milieux porteurs de vie, c’est-à-dire la surface terrestre et les océans, un merveilleux assemblage de protéines est apparu, qui a permis le développement des plantes : le photosystème. Sous l’impact d’un photon, le photosystème est excité et libère un électron. Très réactifs, ces électrons sont ensuite utilisés par les végétaux pour briser la molécule de CO2. Le carbone ainsi débarrassé des atomes d’oxygène est incorporé à la matière vivante dont il est le principal constituant. On l’appelle alors carbone organique, par référence aux organismes qui en sont constitués. Le carbone organique est instable en présence d’oxygène avec lequel il se combine pour redonner du gaz carbonique et de la chaleur.
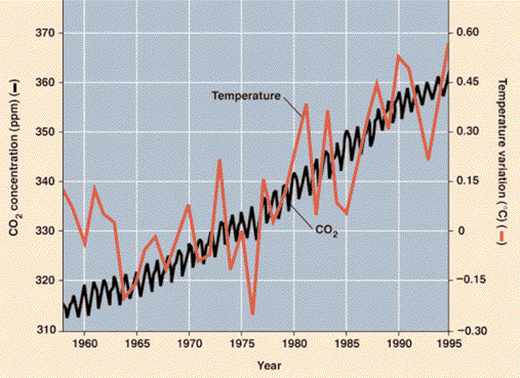
 Aujourd’hui, on a besoin de récupérer cette chaleur pour soutenir l’activité humaine, en brûlant très rapidement (en regard à la lenteur de leur formation) les produits de la photosynthèse ancienne que sont la houille et le pétrole. Le rejet annuel de gaz carbonique est significatif (environ 6 GT/an, soit 5 % des flux naturels échangés entre atmosphère et océan par exemple). Son effet cumulé contribue au renforcement de la couche atmosphérique de gaz à effet de serre dans l’atmosphère, et, par suite, à l’augmentation de la température (on estime que la température moyenne de la planète a augmenté de 0,7 °C au cours du XXe siècle).
Aujourd’hui, on a besoin de récupérer cette chaleur pour soutenir l’activité humaine, en brûlant très rapidement (en regard à la lenteur de leur formation) les produits de la photosynthèse ancienne que sont la houille et le pétrole. Le rejet annuel de gaz carbonique est significatif (environ 6 GT/an, soit 5 % des flux naturels échangés entre atmosphère et océan par exemple). Son effet cumulé contribue au renforcement de la couche atmosphérique de gaz à effet de serre dans l’atmosphère, et, par suite, à l’augmentation de la température (on estime que la température moyenne de la planète a augmenté de 0,7 °C au cours du XXe siècle).
Cependant, lorsque l’on établit l’inventaire cumulé de CO2 dans l’atmosphère aujourd’hui, et que l’on compare au stock brûlé depuis cent cinquante ans, on ne retrouve que la moitié de ce stock. Cela signifie qu’une partie de ce CO2 (dit » anthropique ») a été réabsorbé par la biosphère continentale ou par l’océan…
Reste à déterminer dans quelles proportions ces deux réservoirs réagissent à cet ajout de carbone : en d’autres termes, comment ils se réorganisent face à cette perturbation des flux naturels.
Comprendre les réactions de l’océan (donc, fondamentalement, son fonctionnement) est un des objectifs que se sont fixés les biogéochimistes marins.
Or l’océan est un milieu physique, chimique et biologique, ce que nous illustrons ci-après. Pour comprendre son rôle dans le cycle du carbone il nous faut donc quantifier tous les transports : celui par l’eau (courants marins…), celui par la vie (biologie marine) ainsi que les transferts de la phase dissoute à la phase » particule vivante » (et réciproquement) qui passe par la présence de bactéries, les équilibres chimiques et la présence plus ou moins transitoire d’espèces chimiques et organiques dissoutes.
L’océan et l’atmosphère échangent en permanence du CO2
L’interface entre l’océan et l’atmosphère est traversée par un flux de gaz carbonique qui tend à égaliser les pressions partielles de CO2 dans ces deux milieux. Dans l’atmosphère, la pression partielle de CO2 est une fonction simple de la concentration en CO2 et de la pression atmosphérique, toutes deux étant relativement peu variables. Dans l’océan, c’est un peu moins simple, pour deux raisons :
- d’une part le carbone oxydé s’y présente sous trois formes : le gaz carbonique CO2 dissous et les bicarbonates HCO3- et carbonates CO32-. Ces deux dernières espèces chimiques sont le produit de la dissociation acide du gaz carbonique après sa dissolution dans l’eau, selon l’équilibre 2 HCO3- ⇔ CO32- + CO2 + H2O. (La somme » CO2 dissous, ions carbonates et bicarbonates » est appelée carbone minéral en français, par allusion aux carbonates qui abondent dans les roches, alors que les Anglophones en l’appelant » inorganic carbon » mettent en avant la référence à la vie.) ;
- d’autre part, la solubilité du CO2 dans l’eau intervient aussi : lorsqu’elle augmente (essentiellement lorsque l’eau se refroidit), la pression partielle de CO2 diminue, et inversement. Le réchauffement ou le refroidissement de l’eau au cours de sa circulation vont donc déterminer pour une bonne part l’échange entre l’océan et l’atmosphère.
Prenons par exemple une masse d’eau qui, du fait de la circulation océanique, est remontée à la surface de l’océan au large de l’Angola (on appelle ces zones de remontée d’eau des » upwellings »). Cette eau est très chargée en carbonates et sa pression partielle est élevée. Elle donne donc du CO2 à l’atmosphère, et ceci se prolonge puisqu’elle dérive vers l’équateur et vers le Brésil, en se réchauffant sous un fort soleil. Cette eau a de bonnes chances de passer au nord du Brésil, et dans la mer des Caraïbes, à force de céder du CO2 à l’atmosphère, elle aura à peu près atteint l’équilibre. Commence alors sa dérive vers le nord avec le Gulf Stream. Là, l’eau se refroidit, la solubilité du CO2 augmente, et notre eau va donc absorber du CO2 atmosphérique.
© 1999 ADDISON WESLEY LONGMAN, INC.
Avant que commence le rejet massif de CO2 dans l’atmosphère par l’activité humaine, le bilan de tels échanges était nul. Actuellement, comme la pression partielle de CO2 dans l’atmosphère augmente, un flux » anthropique » s’est instauré, de l’atmosphère vers l’océan. Notons que ce flux est amplifié (par un facteur 10 environ) par l’équilibre illustré par l’équation chimique ci-dessus : en effet, lorsque du CO2 pénètre dans (ou sort de) l’océan, cet équilibre en annule à peu près les 9⁄10e, de telle sorte que l’écart de pression partielle entre les deux milieux persiste beaucoup plus longtemps que si l’océan n’était pas un milieu ionisé riche en carbonates.
Nous illustrons ainsi que le carbone est transporté par la circulation générale océanique, de telle sorte que tout changement de celle-ci en réponse aux modifications du climat induira un changement du contrôle du CO2 par l’océan. Le cycle du carbone est donc étroitement lié à l’évolution de ce premier maillon : le transport des espèces.
Au contraire de la biosphère terrestre, la surface de l’océan s’ouvre sur un immense réservoir : l’océan profond
L’océan est le siège de la photosynthèse (qui fixe le carbone dans les produits de la vie marine). L’énergie produite par la combustion du carbone organique est aussi utilisée par les organismes pour entretenir leurs réactions chimiques, se déplacer, se reproduire, etc. Ce processus de récupération de chaleur (ou d’énergie) par les organismes en brûlant le carbone organique s’appelle la respiration.
Entre la photosynthèse et la respiration, la forme organique ne représente donc qu’un état transitoire du carbone, qui chemine de proies en prédateurs via une cascade d’organismes. Les déchets organiques de cette chaîne sont eux aussi peu à peu oxydés en présence d’oxygène. Comparé à l’énorme quantité de carbonates des roches ou des océans, le monde vivant et ses produits dégradés offrent des capacités de stockage modestes. Leur combustion immédiate suffirait toutefois pour quadrupler la concentration en CO2 de l’atmosphère.
Plus réaliste, et au centre des préoccupations des biogéochimistes, le cycle du carbone se fait selon une chaîne de réactions qui va de la photosynthèse à la respiration, orchestrée par une multitude d’organismes qui ont chacun leur propre réactivité face au climat et à ses changements. Vis-à-vis de ce cycle, les océans présentent des analogies avec ce qui se passe sur les terres émergées pour la biosphère terrestre, mais ils ont aussi des caractéristiques qui leur confèrent un rôle climatique particulier.
Tout jardinier, même s’il n’est qu’amateur, et surtout s’il cajole un tas de compost dans un coin, a une idée très correcte du cycle du carbone. Il sait que la masse végétale issue de la photosynthèse à la belle saison, qu’elle soit ou non dévorée par les insectes et les limaces, finit en grande partie sur le sol où les micro-organismes achèvent son pourrissement. Une partie se retrouve enfouie dans les premiers centimètres du sol et devient humus, pour le plus grand bien des plantes l’été suivant, et on aide en cela en enfouissant cette masse végétale par labour. Entretenir l’humus est une préoccupation permanente, car cet humus est rapidement oxydé en CO2 dans un sol trop aéré dès qu’il fait chaud.
Si un arbre pousse, du carbone est stocké pour des dizaines, voire des centaines d’années, dans le bois qui le constitue. Tout cela peut prendre place dans un jardinet. Enfin, le gaz carbonique est là, disponible, dans l’air ambiant, mais disposer d’eau en quantité suffisante est certainement la principale clé du succès.
Au contraire, dans l’océan, l’eau ne manque jamais, mais elle est très pauvre en sels nutritifs, et c’est l’abondance de ces sels nutritifs, variable selon les régions et les saisons, qui conditionne en premier lieu la capacité de l’océan à transformer ses carbonates en carbone organique. D’autre part, l’océan est animé par des courants, et il est en mélange permanent. À l’origine de ces mouvements, sa fluidité, et les réajustements consécutifs à l’inégale répartition de la chaleur reçue du soleil. Le temps de renouvellement de l’océan est de l’ordre du millier d’années, et le » moteur » de sa circulation globale est l’enfoncement des eaux de surface au voisinage des pôles par suite de leur refroidissement et de l’accroissement de leur densité qui en résulte.
Dans le long circuit qui s’en suit, au cours duquel l’eau froide profonde se dirige vers l’équateur, puis remonte ensuite de façon diffuse, les substances dissoutes, et en particulier les sels nutritifs, sont transportés de manière passive. Si on ajoute à ces conditions la diffusion turbulente, les substances dissoutes dans l’océan devraient être réparties de façon uniforme. Ce n’est pas le cas, car la matière organique élaborée à partir de la photosynthèse est pour une bonne partie organisée en cellules vivantes, puis en débris, et ces entités ont une densité qui, dans la plupart des cas, est légèrement supérieure à celle de l’eau de mer.
En s’enfonçant vers les fonds océaniques, elles retirent de l’eau de surface du carbone, de l’azote et du phosphore dans les proportions 1 : 6,8 : 16, qui sont en moyenne les proportions dans lesquelles ces éléments se trouvent dans la matière vivante. Au cours de leur longue descente, ces particules sont soumises à une dégradation par l’action des bactéries, puis peu à peu oxydées pour revenir aux formes initiales : carbonates, nitrates et phosphates. Quoique faible, ce flux suffit à instaurer dans l’océan un équilibre caractérisé par une couche superficielle éclairée, où l’énergie des photons pourrait permettre la photosynthèse de la matière organique si des sels nutritifs étaient présents (mais le plus souvent, il n’en reste pratiquement pas, drainés qu’ils ont été par la sédimentation des particules), et par une couche profonde où ces sels nutritifs sont abondants, mais où les photons ne parviennent pas.
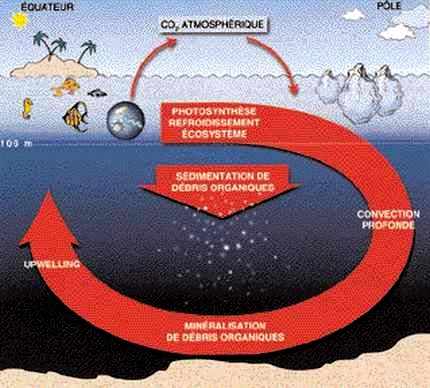
Le cycle du carbone dans l’océan.
Cet équilibre régit une grande partie de l’océan mondial. Il est la règle dans les vastes gyres subtropicaux qui sont animés par les vents alizés aux basses latitudes, et par les vents d’ouest aux latitudes tempérées. La vie se concentre alors à la frontière entre les deux domaines, en profitant de la lente remontée, diffuse ou turbulente, des sels nutritifs, et du faible flux de photons qui y parvient. Les régions soumises à ce régime sont dites oligotrophes (du grec régime maigre), et la pluie de particules qui sédimentent est peu intense.
Mais dans certaines régions, ou à certaines saisons, la conjugaison des sels nutritifs et de la lumière s’opère, et la vie prolifère. Il s’agit des régions situées à l’est des océans tropicaux, où l’eau profonde remonte vers la surface sous l’effet des upwellings (Mauritanie, Benguela, Pérou, Californie), ou bien des moyennes et hautes latitudes lorsque, après l’hiver au cours duquel le refroidissement superficiel a donné lieu à une augmentation de la densité, et à un mélange avec l’eau profonde, le retour du soleil permet une stabilisation de la couche superficielle et amène les photons qui faisaient défaut. Alors, l’océan » grouille de vie » (pêcheries de Mauritanie, du Pérou, de Terre-Neuve), et c’est une véritable averse de particules organiques qui se dépose sur le fond de l’océan.
Cette exportation de matière organique vers la profondeur s’accompagne d’une diminution de la concentration en carbone minéral de la couche superficielle, éclairée, de l’océan. Cette concentration peut ainsi, après la poussée de plancton du printemps aux latitudes tempérées, passer de 2 100 à 1 800 micromoles par kg. Ce n’est pas là une réduction dramatique, mais les carbonates font l’objet d’un équilibre en mer entre le gaz carbonique dissous, l’ion carbonate CO32-, et l’ion bicarbonate HCO3-, ce dernier étant le plus abondant, de telle sorte que lorsque deux ions bicarbonate sont fixés par photosynthèse, une mole de gaz carbonique et un ion carbonate viennent les remplacer. L’effet sur la pression partielle de CO2 à la surface de l’océan est fort du fait de la solubilité de ce gaz, et ainsi, alors que la pression partielle de CO2 est de l’ordre de 400 microatmosphères (µatm) à la surface de l’Atlantique Nord en hiver, elle passe à environ 300 µatm après la poussée printanière de plancton. Or, l’échange de gaz carbonique entre l’océan et l’atmosphère obéit à un rappel vers l’équilibre entre ces deux milieux, modulé par la vitesse du vent et par la différence de pression partielle pCO2(mer) – pCO2(air).
Mesurer les flux : un véritable enjeu
Une approche simple a guidé les pas des océanographes biogéochimistes jusque vers 1990 : constatant d’une part que la disponibilité en nitrates conditionnait l’abondance du phytoplancton et son taux de croissance, et d’autre part que les deux composants principaux de la matière vivante, le carbone et l’azote, s’y trouvaient dans un rapport C/N = 6,6, l’étude du cycle du carbone a été calquée sur celle du cycle de l’azote. La pertinence de cette approche était évidente : la présence ou l’absence de nitrates est la condition sine qua non de la croissance du phytoplancton, et de plus, la mesure de la concentration en nitrates est beaucoup plus aisée que celle des carbonates.
L’épuisement total en nitrate est en effet l’état vers lequel tendent (et qu’atteignent en général) les eaux superficielles de l’océan. Sous ces hypothèses simples, il suffisait donc de représenter au moyen de modèles de circulation océanique l’apport de nitrate vers les couches éclairées proches de la surface, puis de représenter la consommation de ces nitrates par le phytoplancton en se basant sur des mesures de flux biogéochimiques réalisées sur le terrain. La fixation biologique de carbone (ou puits biologique de carbone) pouvait être déduite de celle des nitrates en la multipliant par 6,6, facteur dénommé » rapport de Redfield » du nom de celui qui a le premier établi la valeur des rapports dans lesquels les éléments sont mis en jeu par les processus biologiques en mer. Cette apparente simplicité cache tout de même de nombreuses difficultés.
On ne sait pas, ou mal, mesurer la plupart des flux biologiques, qui, pour la plupart, s’effectuent en même temps dans les deux sens. Par exemple, le phytoplancton respire en même temps qu’il réalise la fixation de carbone par photosynthèse. Ou bien encore, le zooplancton qui broute le phytoplancton rejette dans ses résidus de digestion des sels nutritifs qui sont de nouveau assimilés par le phytoplancton, sans donner lieu à une exportation de carbone en particules vers la profondeur.
D’une façon générale, l’écosystème océanique tend à conserver les éléments qui lui sont indispensables, l’exemple le plus remarquable étant celui de la » boucle microbienne » qu’on peut schématiser de la manière suivante : le phytoplancton de petite taille est brouté par le microzooplancton qui excrète de l’urée, laquelle donne rapidement de l’ammoniaque qui est assimilée par le même petit phytoplancton, fermant le cycle. Les possibles déchets, et cellules mortes, sont attaqués par les bactéries qui restituent de l’ammoniaque.
Cette boucle microbienne est active dans la quasi-totalité de l’océan mondial où elle représente une partie importante de l’activité biologique. Très peu de matière s’en échappe, et la mesure des flux y est très difficile dans la mesure où on ne sait pas séparer dans l’eau de mer le picophytoplancton du microzooplancton ou des bactéries.
L’instrument qui devrait théoriquement le mieux permettre d’estimer le puits biologique de carbone est le piège à particules, qui, à l’instar d’un pluviomètre, capture tout ce qui tombe sur une surface donnée. Placé sous la couche éclairée, il mesurera le flux de particules exportées par l’écosystème de cette couche. Placé à proximité du fond de l’océan, il mesurera le flux qui parvient au sédiment et dont une partie sera enfouie pour des temps géologiques. Entre les deux : la dégradation et la reminéralisation de ces particules par les bactéries qui les accompagnent.
Mais il n’y a pas d’instrument miracle : les pièges fonctionnent mal (essayez dans une bourrasque de neige de mesurer la quantité qui tombe au moyen d’un verre tenu à la main !) ; de plus, une partie importante du puits biologique de carbone leur échappe : c’est celle qui se fait sous forme de molécules organiques dissoutes, qui suivent les masses d’eau sans sédimenter, résistent longtemps à l’oxydation, et peuvent finalement être entraînées avec les eaux, lorsque celles-ci plongent sous l’effet d’un refroidissement ou d’une convergence de courant.
Une diversité d’espèces qui correspond à une diversité de fonctions
Pour imparfaits qu’ils soient, ces pièges à particules confirment toutefois des résultats établis à partir de bilans saisonniers de carbone et d’azote dans les eaux superficielles, qui montrent que les puits biologiques de carbone et d’azote se font la plupart du temps dans un rapport supérieur à la valeur 6,6 établie par Redfield.
Dans les très vastes gyres subtropicaux oligotrophes par exemple (c’est-à-dire le centre des bassins océaniques, entre 10° et 35° de latitude), un bilan de la diminution des carbonates et des nitrates dans la couche de surface entre la fin de l’hiver et l’automne fait apparaître que pour chaque mole de nitrate consommée, c’est davantage que 6,6 moles de CO2 qui disparaissent. La valeur de ce rapport dépend de façon mal connue de l’assemblage d’espèces qui constituent l’écosystème. Déduire par un simple rapport le cycle du carbone de celui de l’azote en donne donc une image qui ne correspond pas à la réalité. Il existe en particulier deux processus biologiques qui sont d’une importance moindre que la photosynthèse, mais dont la prise en compte est nécessaire pour bien représenter les flux de matière dans l’océan : la biocalcification et la diazotrophie.
La biocalcification est la fabrication de pièces calcaires par certains organismes. En associant sous forme de calcaire insoluble un ion carbonate CO32- à un ion calcium Ca2+, elle déplace (ici vers la droite) l’équilibre des carbonates
2 HCO3- ⇔ CO2 + H2O + CO32-.
En dégageant du CO2, elle tend aussi à donner un rôle de source à l’océan vis-à-vis de l’atmosphère, et ce rôle est renforcé par la diminution d’alcalinité (équivalente à une augmentation de pH : l’ajout d’acide dans une solution de carbonates, c’est bien connu, en dégage ces carbonates sous forme de CO2). Les pièces calcaires ainsi formées finissent par s’enfoncer vers les fonds marins dont elles constituent une partie parfois importante.
Même lorsqu’elles se dissolvent partiellement ou entièrement au cours de leur descente, leur évasion de la couche superficielle de l’océan représente un puits de carbone, puisqu’il s’agit de carbone qui n’est plus en contact avec l’atmosphère pour des durées longues, mais la diminution de l’alcalinité qui s’en suit entraîne paradoxalement une augmentation de la pression partielle de CO2, dont l’effet premier est d’entraîner une évasion (ou une invasion moindre) du CO2 de l’océan.
Du fait des parties solides qui sont produites, on désigne parfois ce processus sous le nom de pompe dure de carbone, par opposition avec la pompe biologique qui est basée sur la production de tissus vivants mous. Les principaux organismes qui fabriquent des pièces calcaires sont les coccolithophoridés, les foraminifères et les ptéropodes. Les premiers sont des algues dont le diamètre est compris entre 2 et 3 microns, et qui prolifèrent parfois de manière importante, notamment dans l’Atlantique Nord au mois de juin.
Les foraminifères sont des protozoaires qui font partie du règne animal et qui se fabriquent une coquille calcaire. Il en existe plusieurs espèces avec une répartition assez large. On les retrouve dans les sédiments où leurs préférences écologiques actuelles leur confèrent un rôle d’indicateurs des conditions passées. En particulier, les ions HCO3- qui participent à la réaction ci-dessus et dont l’isotope 13 du carbone est plus ou moins délaissé lors de la réaction de biocalcification en fonction de la température de l’eau de mer. Leurs coquilles dans les sédiments anciens constituent donc des paléothermomètres. Les ptéropodes sont des mollusques pélagiques.
La diazotrophie désigne la propriété qu’ont certaines algues de se procurer l’azote qui leur est nécessaire à partir de molécules d’azote N2 dissoutes dans l’eau. Par rapport aux réserves de nitrate existantes, les disponibilités de N2 sont pratiquement infinies, de telle sorte que l’élaboration de matière vivante est, dans ce cas, non pas freinée par la rareté des nitrates, mais plutôt par celle des phosphates, et aussi par celle du fer. Ce sont principalement les » Trichodesmium « , des algues cyanophycées qui forment des filaments de près de 1 mm de longueur, qui possèdent cette capacité. On les trouve parfois en abondance dans les mers tropicales, cette abondance étant un effet de leur flottabilité positive et de convergences de vents.
Alors qu’une photosynthèse accompagnée par l’assimilation de nitrate n’a pas d’influence sur le stock d’azote de l’océan, la diazotrophie entraîne un gain net d’azote, et une quantité d’azote accrue dans l’océan permet de mobiliser sous forme organique une plus grande quantité de carbone. La diazotrophie, quoique mettant actuellement en jeu des quantités d’azote modestes, est donc de nature à augmenter l’efficacité de la pompe biologique de carbone.
Il existe toutefois un processus opposé : la dénitrification, qui se produit dans des masses d’eau très appauvries en oxygène. De telles masses d’eau se rencontrent en profondeur dans les régions extrêmement productives comme l’upwelling du Pérou ou la mer d’Arabie. Alors, l’oxygène dissous dans l’eau ne suffit plus pour oxyder l’énorme quantité de matière organique produite, et par le biais de certaines bactéries qui en possèdent la capacité, l’oxygène indispensable est pris aux ions NO3-, avec libération de N2.
Diazotrophie et dénitrification sont totalement indépendantes, ont lieu dans des régions disjointes, mais leur équilibre définit cependant pour une bonne part l’évolution du stock de nitrate de l’océan.
Les coccolithophoridés qui accomplissent la biocalcification, ainsi que les Trichodesmium qui sont diazotrophes, possèdent des propriétés optiques particulières : les pièces calcaires chez les premiers, et des bulles de gaz chez les seconds, diffusent la lumière et donnent à l’océan une coloration particulière, très éloignée du bleu traditionnel. Ceci fournit le moyen de les détecter par satellite, et quantifier ces deux processus par télédétection de la couleur de la mer est actuellement une voie de recherche.
De manière générale, la télédétection de la couleur de l’océan permet de quantifier sa concentration en chlorophylle, et grâce à la puissance de cet outil, capable d’observer l’océan global en quelques jours, pendant plusieurs années, il est possible d’estimer en permanence la photosynthèse. La chlorophylle est en effet un des éléments du photosystème des algues, et on connaît de mieux en mieux les paramètres de modèles de photosynthèse forcés par la lumière et par la concentration en chlorophylle.
Depuis 1997, un satellite américain, SeaWiFS, fournit de telles données. Le relais devrait être pris vers la mi-2002 par un capteur européen, MERIS, puis par un capteur français, POLDER. L’utilisation de modèles de circulation océaniques couplés à des modèles biogéochimiques et prenant en compte l’information fournie par ces satellites est une stratégie très lourde mais qui offre la perspective de pouvoir comprendre et correctement représenter le puits biologique de carbone.
En plus de l’azote comme élément limitant pour la synthèse de matière organique, nous aurions pu évoquer la silice, qui est indispensable pour la croissance des diatomées, qui en font leur squelette et sont les algues les plus efficaces en termes d’enfouissement de carbone organique vers la profondeur. Nous avons aussi évoqué le phosphore, et surtout le fer, indispensable à haute dose pour la diazotrophie.
Le fer est très abondant dans l’environnement terrestre, dans les sols, mais il est très peu soluble et comme cela a été montré pendant les années 1990, c’est lui qui limite probablement le plus le puits biologique de carbone. Des atomes de fer font en effet partie de certaines protéines du photosystème, et sont indispensables à la croissance du phytoplancton. Comme le fer est très peu soluble dans l’océan, sa disponibilité dépend finalement des retombées de poussières atmosphériques. C’est pour cette raison que le Pacifique équatorial, ou que l’océan Antarctique, présentent en surface des concentrations élevées en nitrates, qui, paradoxalement, ne sont utilisés que très lentement par la photosynthèse. La raison est l’éloignement de ces régions par rapport aux continents, et, consécutivement, la rareté des retombées de poussières océaniques.
Une rétroaction du changement climatique sur les espèces ?
La pompe biologique de carbone par l’océan est donc un système à plusieurs composantes (photosynthèse, biocalcification, diazotrophie, respiration, sédimentation, disponibilité en nitrate, en phosphate, en silice, en fer), et cette complexité est accrue par la diversité des acteurs qui interviennent.
Les milliers d’espèces qui constituent le plancton ont chacune un potentiel génétique qui définit leurs capacités de croissance, leurs besoins, leur adaptabilité, leurs interactions avec leurs prédateurs ou leurs proies. Dans l’état présent de l’océan, sous le climat actuel, elles mettent en œuvre la pompe biologique qui contribue, dans une certaine mesure, à réduire l’accumulation de CO2 dans l’atmosphère. Dans un climat modifié, le peuplement planctonique s’adaptera, et c’est un assemblage d’espèces différent qui mettra en œuvre cette pompe biologique. Prévoir la tendance qui s’instaurera n’est pas facile, et le premier pas consiste sans doute à comprendre comment le climat actuel, et la circulation océanique qui en découle, contrôlent le peuplement actuel.