La modulation cérébrale implantée en psychiatrie

Repères
Repères
La méthodologie d’investigation neurophysiologique par stimulation électrique connaît un essor à partir de 1930 avec le neurochirurgien Wilder Penfield. Avec la stimulation électrique, chaque cas de neurochirurgie ouvre maintenant potentiellement un temps d’exploration fonctionnelle. Lors d’interventions neurochirurgicales sur des épileptiques, on réalise systématiquement des séries de stimulation du cortex provoquant des signes cliniques que le neurologue observe tout en interrogeant le malade conscient. Cette méthodologie du modèle expérimental humain de signes cliniques transforme la temporalité des observations.
Contrairement à la lésion, la stimulation électrique par sa réversibilité permet la reproduction du modèle expérimental sur un même sujet humain ou animal. C’est dans ces conditions empiriques et expérimentales d’une stimulation électrique comme technique d’investigation clinique et de recherche dans une finalité thérapeutique qu’est née la stimulation cérébrale profonde (SCP).
La découverte empirique dans les années soixante par plusieurs équipes que la stimulation à haute fréquence du thalamus dans le tremblement possède les mêmes effets que la lésion ne trouvera son application thérapeutique que dans les années quatre-vingt avec l’invention de la SCP par le neurochirurgien français Alim Louis Benabid. Il sera le premier, à partir de cette observation, à penser un système de stimulation chronique implanté sur le malade.
La stimulation deviendra alors chronique et profonde, prenant le relais de la chirurgie lésionnelle dans le tremblement.
Implantation stéréotaxique
Concrètement, une opération chirurgicale est requise pour implanter généralement une électrode dans chaque hémisphère cérébral, les électrodes étant elles-mêmes raccordées à un boîtier d’alimentation, au moyen d’un câble passant sous la peau du patient. Des impulsions électriques d’une fréquence généralement comprise entre 80 et 150 hertz sont ainsi délivrées à diverses zones du cerveau, choisies en fonction de leur implication dans le trouble concerné.
Une technique qui se répand
|
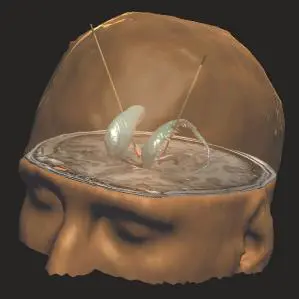
L’ensemble du crâne avec les noyaux caudés et deux électrodes implantées dans les noyaux sousthalamiques. Image : Luc Mallet/Jérôme Yelnik/Éric Bardinet(Inserm, CNRS-INRIA). |
Les progrès de l’implantation stéréotaxique (réalisée à l’aide de systèmes de coordonnées tridimensionnelles permettant de repérer avec fiabilité l’emplacement des diverses zones cérébrales chez un patient) ont permis d’appliquer ce principe à une foule de cas pathologiques, de la maladie de Parkinson au syndrome de la Tourette, en passant par les troubles obsessionnels compulsifs ou la dépression.
Quels effets en retire-t-on ? Généralement, une amélioration assez nette de l’état du patient. La question qui se pose aujourd’hui est, entre autres, celle du lieu d’implantation. Et cette question rejoint celle du modèle théorique sur lequel on s’appuie pour comprendre divers troubles mêlant les symptômes moteurs et affectifs, voire cognitifs.
Des moyens d’action à plusieurs niveaux
Aujourd’hui, le cadre théorique dans lequel on s’inscrit pour comprendre des pathologies aussi diverses que le syndrome de la Tourette, la maladie de Parkinson ou les troubles obsessionnels compulsifs fait intervenir des circuits que l’on nomme cortico-sous-corticaux, c’est-à-dire reliant les divers territoires du cortex à des zones plus profondes du cerveau.
Ces maladies sont généralement caractérisées par des difficultés d’exécution des mouvements, parfois accompagnées de troubles affectifs. Ce caractère composite s’explique si l’on part du point de vue que le contrôle des mouvements fait intervenir une part purement motrice mais également une part affective et un volet plus » mental » ou purement cognitif. Ces trois aspects sont pris en charge par des circuits en boucle dans le cerveau reliant les divers cortex (cortex moteur pour la préparation des mouvements, cortex associatif pour la prise en compte de l’environnement, cortex limbique » émotionnel ») et les structures profondes.
La plupart des opérations de stimulation profonde ciblent un des maillons de cette chaîne, qu’il s’agisse du pallidum pour la maladie de Gilles de la Tourette, du striatum ventral pour les addictions ou la dépression, du noyau subthalamique pour la maladie de Parkinson ou les troubles obsessionnels compulsifs.
Comment interpréter cette variété de cibles, et leur spécificité ? Le cas du noyau subthalamique est particulièrement éclairant.
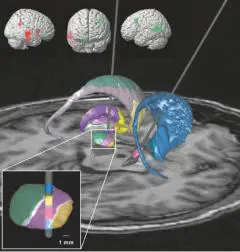
Dans une étude de cas de maladie de Parkinson, nous avons constaté que la stimulation du noyau subthalamique au moyen d’électrodes implantées dans le cerveau du patient avait des effets aussi bien sur ses mouvements que sur son humeur. En outre, il était possible de se concentrer sur les effets moteurs en évitant les effets sur le plan de l’humeur, en fonction de la profondeur à laquelle était délivré le courant électrique, au millimètre près.
Cela suggérait que certaines parties du noyau subthalamique (qui est pourtant une structure de petites dimensions) étaient impliquées dans le contrôle des mouvements, alors que d’autres participaient à l’état affectif. Aujourd’hui, l’on pense que l’ensemble de la boucle neuronale décrite plus haut comporte trois subdivisions parallèles, un circuit émotionnel, un circuit moteur et un circuit associatif, engagés dans la prise de décision.
Ces trois circuits sont en quelque sorte accolés les uns aux autres et convergent au niveau du noyau subthalamique, ce qui fait de ce dernier un levier d’action privilégié où il est possible d’agir sur ces trois versants du psychisme que sont la cognition, l’émotion et la motricité.
Des avancées thérapeutiques considérables
Récemment, l’identification de dysfonctionnement de circuits cérébraux profonds dans le trouble obsessionnel compulsif (TOC), qui touche 2 % de la population, a conduit à proposer des traitements chirurgicaux au moyen de techniques de modulation cérébrale implantée pour les patients les plus atteints. Suite à des avancées récentes portant sur l’organisation fonctionnelle des ganglions de la base, nous avons élaboré un protocole multicentrique contrôlé évaluant l’efficacité de la stimulation à haute fréquence du noyau sous-thalamique et montré que cette technique pourrait représenter une alternative thérapeutique pour ces patients à très fort handicap, représentant environ 12 000 personnes en France.
Les défis du futur
Malgré ses résultats prometteurs, la technique de stimulation profonde reste entourée de nombreuses inconnues. Quelle est l’action précise du courant électrique sur les neurones des différentes zones cérébrales ciblées ? Comme toute technique pionnière, celle-ci offre tout à la fois un bénéfice thérapeutique et de nouvelles directions de compréhension des fonctions cérébrales et psychiques. C’est en partie grâce à la stimulation profonde que l’on conçoit aujourd’hui l’affect et l’action comme étroitement liés, et que l’on peut proposer des hypothèses de dysfonctionnement neuronal pour expliquer les obsessions. Quant à savoir exactement pourquoi l’injection d’un courant électrique artificiel dans une boucle neuronale de ce type concourt à rétablir l’équilibre subtil sur lequel repose l’harmonie entre les pensées, les actes et les émotions, c’est sans doute un des plus grands défis qui nous reste à relever, pour lequel des avancées technologiques restent à concrétiser.

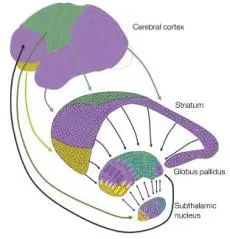 Ganglions de base
Ganglions de base

