Matériaux magnétiques moléculaires

Même si les fibres naturelles, matériaux macromoléculaires d’origine végétale ou animale, ont été utilisées par l’homme depuis la nuit des temps, ce sont les matériaux solides que l’humanité a retenus pour rythmer son histoire (âge de la pierre, du fer, du bronze, du silicium…). Aujourd’hui, les besoins en matériaux légers, biocompatibles, recyclables, aux propriétés nouvelles mais prévisibles, favorisent le développement d’une chimie moléculaire des matériaux fondée sur l’immense flexibilité de la chimie du carbone et des éléments de transition.
Les polymères (chimie macromoléculaire), les cristaux liquides en sont de beaux exemples quotidiens (figure 1). Cette approche moléculaire séduit sans doute pour des raisons de taille (la molécule est l’étape ultime de la miniaturisation de l’objet fonctionnel) mais peut-être surtout parce que la molécule peut être pourvue dès sa conception de l’information nécessaire (structurale, électronique…) pour construire le solide final de structure et de propriétés requises [1]. Dans le domaine du magnétisme, où métaux et oxydes se partagent un marché considérable aux applications multiples, le magnétisme moléculaire [2, 3] représente un champ de recherche en pleine expansion que nous illustrons par quelques exemples.
Jeu de spins, d’électrons, d’orbitales
Le magnétisme moléculaire joue des électrons et des spins à l’aide des grands principes de la science quantique. À chaque électron est associé un spin S = 1⁄2 qui possède un moment magnétique élémentaire, point de départ des propriétés magnétiques. Le couple fidèle d’électrons, à spins antiparallèles, est diamagnétique. Les systèmes à couches électroniques ouvertes sont paramagnétiques et les éléments de transition y jouent un rôle majeur.
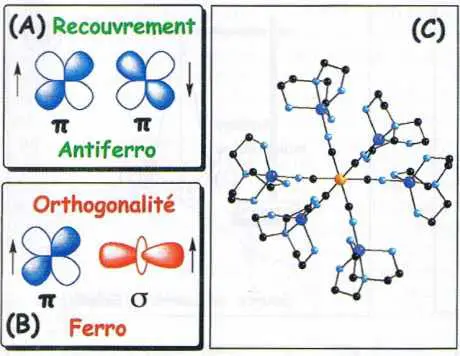
La maîtrise des propriétés magnétiques du système passe par la maîtrise de la symétrie de chaque centre, puis par celle de l’interaction entre électrons célibataires sur deux centres voisins A et B. Lorsque les électrons sont localisés, un modèle quantique simple prévoit [2] que le recouvrement des fonctions d’onde (ou orbitales) décrivant les deux électrons conduit à une interaction antiferromagnétique (spins antiparallèles, spin total ST = SA – SB = 0) (figure 2A) et que l’orthogonalité des deux fonctions d’onde mène à une interaction ou couplage ferromagnétique (spins parallèles, spin total ST = SA + SB = 1) (figure 2B).
L’air que respire le lecteur de La Jaune et la Rouge fournit les deux exemples : le diazote est diamagnétique (SN2 = 0, fort recouvrement entre orbitales des électrons de chaque azote), le dioxygène est paramagnétique (SO2 = 1, orthogonalité des orbitales). Une situation nouvelle et amusante naît quand les orbitales se recouvrent, avec un nombre différent d’électrons sur A et B. Alors ST = SA – SB ≠ 0. Le spin résultant ST est non nul. Paradoxalement, ou dialectiquement, l’antiferromagnétisme engendre un magnétisme résultant. C’est le ferrimagnétisme, idée qui a contribué à valoir le prix Nobel à Louis Néel, récemment décédé.
Nantis de ce modèle théorique simplifié, nous pouvons passer aux applications. Parmi les succès les plus spectaculaires de cette approche rationnelle des propriétés magnétiques des matériaux à précurseurs moléculaires figure l’obtention de molécules de spin très élevé et de » bleus de Prusse » qui présentent des propriétés d’aimants à température ambiante.
Des molécules à spin plus élevé que le gadolinium.….. vers le stockage de l’information sur une molécule
Dans la classification périodique, l’ion qui présente le spin maximum est l’ion gadolinium(III), avec sept électrons célibataires dans les orbitales f, f7, S = 7⁄2.
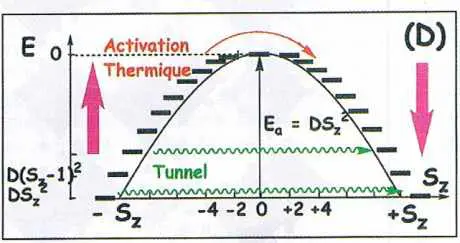
L’application du modèle ci-dessus permet aux chimistes moléculaires de mieux faire ! Voyons comment. Dans le complexe moléculaire octaédrique chromicyanure [CrIII (CN) 6]3-, six ions cyanure entourent un ion chrome(III), d3. Les trois électrons sont dans des orbitales d de symétrie π (t2g) (figure 2A). La réaction de ce complexe avec six complexes du cuivreII, d9, S = 1⁄2, [CuIItren]2+, où le seul électron célibataire de l’ion cuivre(II) est dans une orbitale de symétrie s (eg) (figure 2A), donne un complexe heptanucléaire [CrIII{CN-CuII(tren)}6]9+ où chaque azote du chromicyanure est lié à un cuivre(II) (figure 2B).
Des ions négatifs séparent les molécules les unes des autres. Comme les orbitales du chrome et du cuivre sont orthogonales, l’interaction J[chrome(III)-cuivre(II)] est ferromagnétique. Le spin total est ST = SCr + 6 SCu = 9⁄2, mieux que le gadolinium. La même stratégie ferromagnétique, en remplaçant le cuivre(II) par le nickel(II) (spin SNi = 1), amène à ST = SCr + 6 SNi = 15/2… mieux encore !
Quand, dans l’approche ferrimagnétique, on utilise le manganèse(II), d5, SMn = 5⁄2, l’interaction devient antiferromagnétique. Le spin du complexe [CrIII{CN-MnII (tetren)}6]9+ est alors ST = 6 SMn – SCr = 27⁄2 ! Ce jeu de construction moléculaire est donc intellectuellement satisfaisant. Il est aussi directement lié à la préoccupation de la miniaturisation des éléments de stockage magnétique de l’information.
| Figure 2 |
  |
| Modèle, molécule àhaut spin, anisotropie : vers des molécules-aimants. |
Si le rythme actuel de miniaturisation se maintient, on devrait atteindre l’échelle moléculaire dans un peu plus d’une dizaine d’années… Les chimistes moléculaires s’efforcent donc de construire des éléments (sub)nanométriques » à partir du bas » (ou approche bottom-up), en suivant R. Feynman (« There is plenty of room at the bottom »).
Plus précisément depuis 1993, mes collègues D. Gatteschi, D. Hendrickson, G. Christou et d’autres étudient des molécules polynucléaires (à cœur Mn12 ou Fe8) de spin élevé (S = 10), très anisotropes. Ces molécules refroidies dans un champ magnétique, puis placées en champ nul à très basse température (T < 2 Kelvins), voient leurs moments magnétiques rester alignés dans la direction du champ comme un aimant traditionnel. Mais ici il n’y a pas d’interaction entre les molécules.
La barrière d’anisotropie ∆E (figure 2D) est proportionnelle au carré du spin et à la constante d’anisotropie D, ∆E = DSz2. Pour présenter une barrière de 400 Kelvins où l’orientation des moments serait » robuste » à l’ambiante, il faudrait un spin moléculaire S = 20 et une anisotropie D = 1 K. Ce n’est pas hors de portée… (Une molécule à spin S = 39⁄2 a été caractérisée par une équipe japonaise.) Mais bien des problèmes demeurent sur le chemin de l’enregistrement sur UNE molécule…
Le bleu de Prusse, une vieille connaissance
Un autre exemple, utilisant les mêmes précurseurs moléculaires et la même stratégie, permet de synthétiser des aimants qui s’ordonnent à une température où les applications deviennent possibles (azote liquide et température ambiante). Lorsque l’interaction à courte distance s’exerce dans les trois directions de l’espace jusqu’à l’infini, on obtient à une certaine température critique un ordre magnétique où tous les spins deviennent ordonnés à longue distance : parallèles dans le cas du ferromagnétisme (SA + SB), antiparallèles dans le cas du ferrimagnétisme (|SA – SB|). La température de transition est la température de Curie, TC.
C’est ce qui arrive quand on laisse le chromicyanure libre de se lier dans les trois directions de l’espace avec des ions de transition dans l’eau. C’est une chimie qui date du début du XVIIIe siècle quand Diesbach, drapier berlinois, cherchait à obtenir des pigments pour ses étoffes : en portant du sang de bœuf à ébullition à l’air en milieu basique pendant plusieurs heures, il vit apparaître un pigment bleu, le bleu de Prusse. Le lecteur de La Jaune et la Rouge a précipité ce magnifique pigment en travaux pratiques de chimie, pour caractériser le fer(III), mais de manière plus douce : 3 [FeII(CN)6]4- + 4 [FeIII(H2O)6]3+ → FeIII4[FeIICN)6]3 • nH2O.
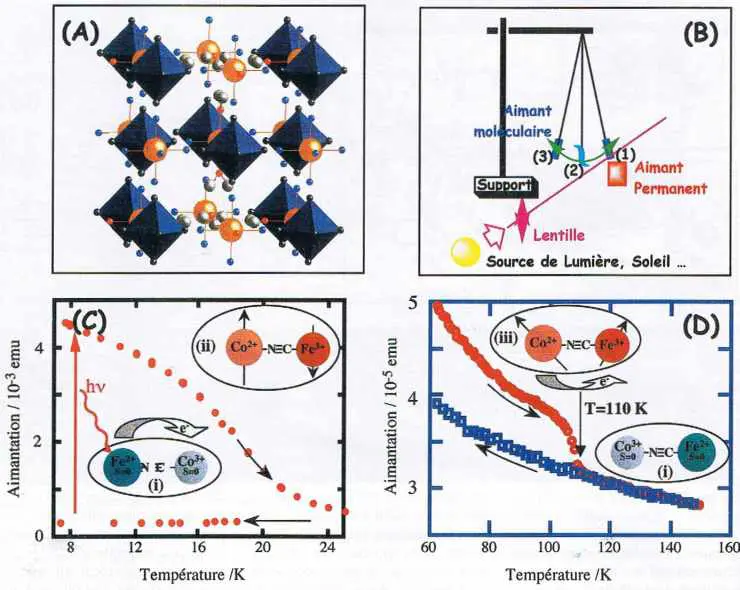
La stœchiométrie du solide résulte de la neutralité électrique : dans l’eau, solvant polaire, ce qui est neutre précipite. La structure est une structure cubique à faces centrées (chlorure de sodium) avec des lacunes puisqu’il y a moins d’ions ferricyanure que d’ions ferriques. Les lacunes se remplissent de molécules d’eau, coordonnées aux ions fer(III) ou liées entre elles par liaisons hydrogène (figure 3A).
Le bleu de Prusse, où les ions paramagnétiques Fe(III) sont distants de plus de 10Å, est un solide paramagnétique. Sa température d’ordre magnétique (ferromagnétique) est très basse (TC = 5,6 Kelvins – K). Mais les analogues du bleu de Prusse offrent :
(i) la possibilité de développer des interactions orbitales dans les trois directions de l’espace ;
(ii) une haute symétrie où les alignements A‑CN‑B permettent un contrôle efficace de la nature et de la valeur de l’interaction entre A et B ;
(iii) la flexibilité de la structure, capable d’accueillir de très nombreux ions paramagnétiques différents et donc de présenter une grande gamme de propriétés magnétiques ;
(iv) la possibilité de modifier le nombre de voisins magnétiques z autour de A avec la stœchiométrie. Ce dernier point est particulièrement important car Néel a montré que la température de Curie est proportionnelle à la fois à l’interaction entre voisins et au nombre de voisins magnétiques.
Des aimants à précurseur moléculaire à température ambiante
Ainsi, en utilisant le couple ferrimagnétique CrIIIMnII, utilisé plus haut pour les molécules à spin élevé, D. Babel a obtenu dans les années quatre-vingt un système ferrimagnétique CsI4MnII4[CrIIICN)6]4, dont la température de Curie TC = 90 K est supérieure à la température de l’azote liquide, palier important vers les applications. L’ion césium assure l’équilibre des charges avec une stœchiométrie Cr1Mn1(ou Cr4Mn4) qui optimise le nombre de voisins z = 6. Au début des années quatre-vingt-dix, nous avons montré que le couple CrIIINiII donne un aimant ferromagnétique CsI4NiII4[CrIIICN)6]4 à la même température de Curie 90 K.
| Figure 3 |
 |
| Analogues du bleu de Prusse : structure et applications [4]. |
Puis, en jouant sur la structure électronique, nous avons augmenté l’interaction antiferromagnétique, en associant au chromicyanure, des ions CrII, SCr = 2 et VII, SV = 3⁄2. C’est une chimie un peu difficile mais les températures de Curie deviennent 240 K dans CrII4 [CrIII(CN)6]8⁄3 et 315 K dans VII4 [CrIII(CN)6]8⁄3. La température ambiante est atteinte, le défi est relevé. Le résultat est le fruit d’une approche rationnelle. Un lecteur attentif aura remarqué que le nombre moyen de voisins magnétiques est z = 4 dans les stœchiométries proposées et ne manquera pas de faire valoir qu’il est possible de mieux faire encore, avec une stœchiométrie CsI4VII4[CrIII(CN) 6]4 où z = 6. Effectivement, une température de 376 K, au-dessus de la température d’ébullition de l’eau, a été mesurée par un chercheur américain, G. Girolami, sur un composé de stœchiométrie très proche. Un autre lecteur attentif fera alors remarquer que puisque le couplage est antiferromagnétique entre CrIII et VII, et que la stœchiométrie est exactement 1⁄1, alors il ne s’agit plus d’un aimant mais d’un solide antiferromagnétique car les spins 3⁄2 du chrome et du vanadium se compensent exactement. Il a raison : en magnétisme moléculaire aussi, la roche Tarpéienne est proche du Capitole [4a, b].
Nous pouvons maintenant abandonner les décomptes fastidieux d’interactions et de spins, et exploiter la possibilité ouverte de passer aux applications pratiques des aimants à précurseurs moléculaires dont la température de Curie est proche de la température ambiante (figure 3B). L’aimant à précurseur moléculaire (TC = 315 K) est placé dans une ampoule dans un gaz inerte (argon) car exposé à l’air, il perd ses propriétés.
Il est suspendu à un point fixe, comme un pendule. Quand il est froid, il est attiré par l’aimant permanent. En ce point, il est réchauffé par un faisceau lumineux (lampe, soleil). Quand sa température dépasse la température d’ordre, il n’est plus attiré par l’aimant et repart vers la verticale. Hors du faisceau, l’air ambiant le refroidit et il est à nouveau attiré : d’où un mouvement oscillatoire où l’énergie lumineuse est transformée en énergie mécanique. Des millions de cycles ont été ainsi effectués sans fatigue, dans une machine thermodynamique qui utilise deux sources d’énergie gratuite, l’énergie solaire et l’air ambiant : sonde thermique, interrupteur magnétique, stockage d’énergie solaire en énergie mécanique.
Jeux de photons et de spins, où la lumière transforme un système diamagnétique en ferrimagnétique, vers des mémoires photomagnétiques réinscriptibles
Un autre exemple spectaculaire des possibilités de ces analogues magnétiques du bleu de Prusse est le ferrimagnétisme photo-induit. Le phénomène a été mis en évidence par l’équipe japonaise de H. Hashimoto en 1996 sur un matériau dont le précurseur est [FeIII(CN)6]3-. Associé au cobalt(II), le ferricyanure peut conduire aux systèmes CoII4FeIII8⁄3, ferrimagnétique (TC = 15 K) et Cs4Co4Fe4, diamagnétique ! Dans ce second composé, le cobalt(II) est soumis à un champ cristallin plus important. Il devient plus réducteur et transfère un électron au fer(III). Dans la paire CoIII-NC-FeII résultante, les deux ions adoptent une configuration électronique où tous les électrons sont appariés dans des orbitales π. La paire et le composé sont diamagnétiques.
L’éclairement en lumière rouge de l’entité CoIII-NC-FeII, dans un film mince d’un composé où le taux de césium est moindre mais bien contrôlé (figure 3C), conduit à un transfert d’électron inverse et à une entité photoexcitée [CoII-NC-FeIII]* de spin non nul. La création de ces entités sous éclairement produit un solide ferrimagnétique en dessous de 20 K. Entre 20 et 110 K, le produit est paramagnétique. Enfin à 110 K (figure 3D), l’activation thermique du transfert électronique redonne des paires CoIII-FeII, diamagnétiques. L’échantillon redevient diamagnétique.
Sans doute les températures d’ordre sont-elles faibles mais il s’agit du premier exemple d’une transition photo-induite diamagnétique-ferrimagnétique et de l’illustration du principe du stockage photomagnétique d’une information sur une mémoire réinscriptible, exemple du potentiel de développement des techniques optiques de stockage de l’information [4c]. La place nous manque pour développer d’autres exemples, en particulier les remarquables propriétés des aimants optiquement actifs énantiomériquement purs obtenus par l’équipe de M. Gruselle dans notre laboratoire où dichroïsme naturel et magnétique donneront naissance à des effets magnéto-optiques nouveaux.
En guise de conclusion
Au-delà des exemples ci-dessus, choisis dans la chimie de notre équipe, la recherche sur de nouveaux matériaux magnétiques moléculaires est très active, au niveau national et international. Le savoir-faire du chimiste en synthèse et la flexibilité de la chimie moléculaire permettent la construction rationnelle de nouveaux objets magnétiques. Nous avons vu que certains matériaux sont capables de présenter plusieurs fonctions en » posant » l’information nécessaire sur les précurseurs, conçus pour la circonstance (magnétisme modulé par la lumière pour l’enregistrement photomagnétique, chiralité…).
Ces objets de plus en plus complexes sont évidemment de plus en plus difficiles à obtenir car leur édification repose sur la maîtrise d’interactions souvent ténues. La thermodynamique, la cinétique ont parfois raison des rêves les plus fous. Néanmoins, le champ progresse, fruit d’une étroite collaboration avec les physiciens maîtrisant des méthodes de physique » lourdes » (basses températures, contraintes, microscopies à effet tunnel, neutrons, synchrotron…) et demain avec des ingénieurs pour la mise en forme et l’utilisation comme matériaux. D’autres lignes de développement existent, plus proches de la biologie (modèles moléculaires de la ferritine et des oxydes magnétiques des organismes vivants…), toujours source d’inspiration et d’espoir.
Tout porte à croire que la » spin-onique » moléculaire que nous venons d’évoquer, sœur de l’électronique moléculaire, sera l’une des composantes actives de la chimi-onique suggérée par J.-M. Lehn.